【文化课学习笔记】【化学】选必三:有机化合物的结构特点与研究方法(下)
【化学】选必三:有机化合物的结构特点与研究方法(下)
如果你是从 B 站一化儿笔记区来的,请先阅读我在第一篇有机化学笔记中的「读前须知」(点开头的黑色小三角展开):链接
有机物命名规则
有机物的命名
有机物结构复杂,种类繁多。为了使每一种有机物对应一个名称,需要按照一定的规则和方法,对每一种有机物进行命名。
烷烃的命名
烷烃的相关介绍
烷烃是一类有机化合物,分子中的碳原子都以碳碳单键相连,其余的价键都与氢结合而成的化合物,属于饱和烃。分为环烷烃和链烷烃两类。 链烷烃的通式为
习惯命名法
根据碳原子数进行命名:
-
碳原子数在 10 以下:依次用甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示。
-
碳原子数在 10 以上:用中文数字表示。
-
遇到同分异构体,即碳、氢原子数目相同时:用正、异、新等来区别。
示例:

系统命名法
【命名步骤】
- 选主链,称「某烷」:含有最多碳原子的链定位主链。碳数相同时,支链最多的链为主链。具体选取规则见下方【主碳链&主碳链的选取规则】。
- 编号位,定支链:需要遵循离支链最近的一端定位
- 写名称:「数字
【命名架构】
位置编号(用阿拉伯数字表示)- 取代基 - 主碳链。
命名时以阿拉伯数字表示取代基或官能团(支链)的位置编号,以中文数字表示取代基(相同支链)的个数,阿拉伯数字与汉字间以短横线「
不同基团,命名时简单在前、复杂在后、相同合并,最后写主链名称。先写支链位置,再写支链名称,简单智联写在前(例如甲基写在乙基前面),多个相同侧链用汉字直接描述数目,比如「
注意:若一个基团上有多个甲基,则每个甲基的位置均需描述出来,例如
二甲基,而不是 二甲基。
例如,下面左图的烷烃,用系统命名法命名为
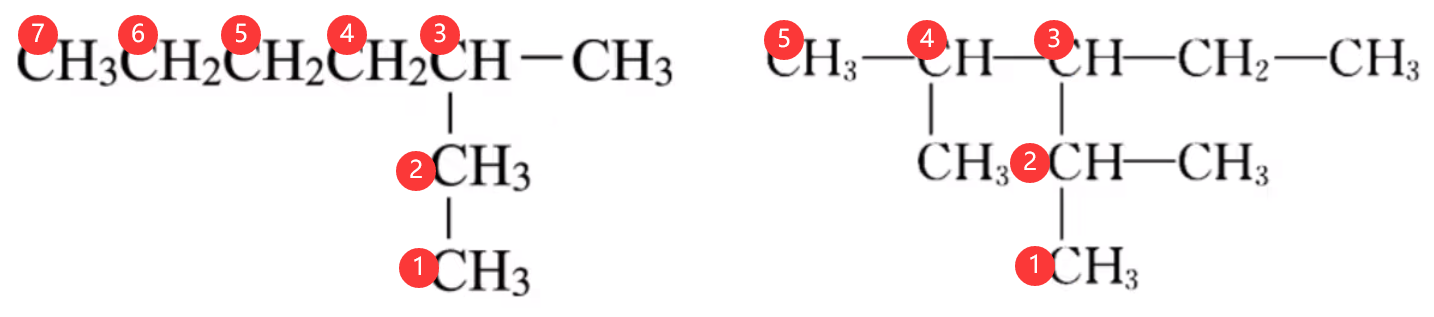
【常见的烃基(烃分子失去一个氢原子,剩余的基团)】
甲烷
乙烷
丙烷 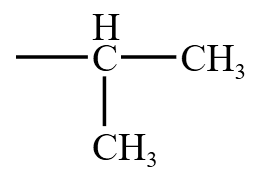 。即正丙基所有碳原子都在主链上,而异丙基有一个碳原子在支链上。
。即正丙基所有碳原子都在主链上,而异丙基有一个碳原子在支链上。
乙烯
苯 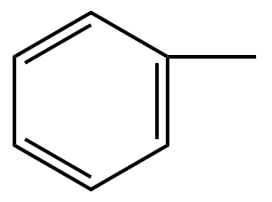 ,一般用
,一般用
注意:取代基也有同分异构体。
【取代基顺序规则】
- 烷基取代基命名顺序由简到繁,比如先命名丙基,再命名异丙基。
- 其它取代基命名,先比较各支链的第一个原子的原子序数大小,例如
【主碳链&主碳链的选取规则】
-
以最长的连续碳链为主碳链,以此主链决定烷烃的基本名称。
-
支链最简原则:当有几个相同长度的最长碳链时,选择含支链最多的一个作为主链。
即选用主碳链时,取代基需要遵循「小而多」,例如,在下图的烷烃中,如果选用左图中标号碳链为主碳链,则取代基有
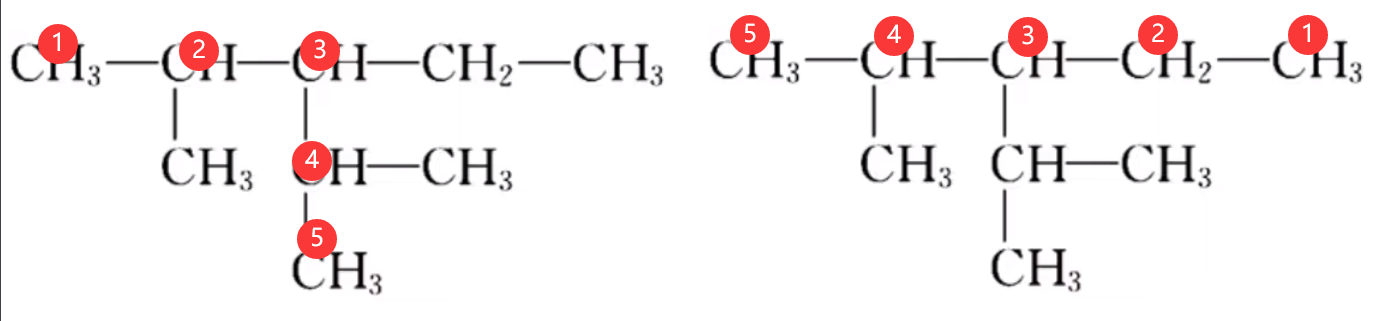
【编号位需要遵循的原则】
编号位要遵循「近」「简」「小」的原则。
-
首先要考虑「近」,即以离支链较近的一端给主碳链原子编号。例如,下图中的烷烃,距离主碳链两端最近的是距离右端第二个碳上的取代基,所以应该从主碳链右端开始编号,命名为
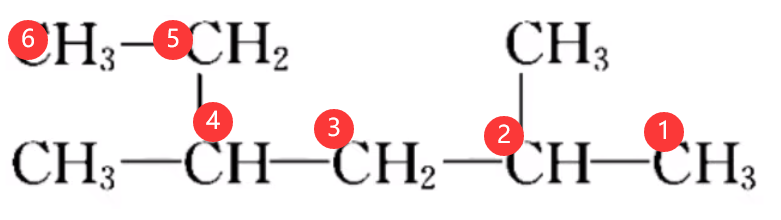
-
同「近」则考虑「简」,即有两个不同的支链,且分别处于距离主链两端同近的位置,则从支链较简单的一端开始编号。例如,下图中的烷烃,距离主链两端的第三个碳上都有一个取代基,左端第三个碳上的乙基支链比右边第三个碳上的甲基简单,所以从左端开始编号,命名为
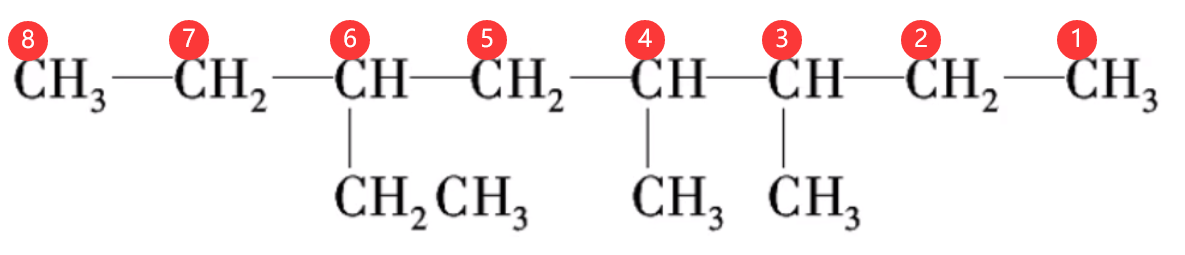
-
若有两个相同的支链,且分别处于距主链两端同近的位置,而中间还有其它支链,从主链的两个方向编号,可得两种不同的编号序列,两序列中各支链位次和最小者即为正确的编号。例如,下图中的烷烃,主碳链从左向右和从右向左得到的分别是
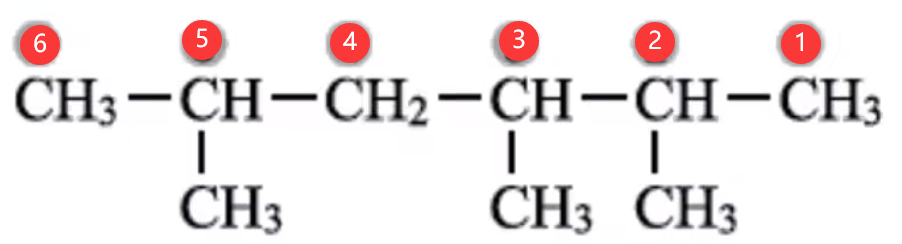
烯烃和炔烃的命名
烯烃和炔烃的相关介绍
烯烃是指含有碳碳双键
炔烃,为分子中含有碳碳三键的碳氢化合物的总称,是一种不饱和的脂肪烃,直链单炔烃的分子通式为
其中烯烃中含有官能团 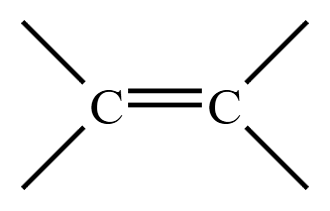 ,炔烃中含有官能团
,炔烃中含有官能团 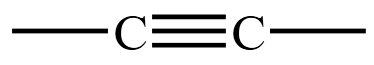 。
。
命名方法
步骤:
- 选主链:将含有碳碳双键或碳碳三键的最长碳链作为主链,成为「某烯」或「某炔」。
- 编序号:从距离碳碳双键或碳碳三键最近的一端对主链上的碳原子进行编号定位。除此之外,编号位仍然满足烷烃的系统命名法中「编号位遵循的规则」。
- 写名称:将支链作为取代基,写在「某烯」或「某炔」的前面,并用阿拉伯数字标明碳碳双键或碳碳三键的位置,写出有机物的名称。格式为「数字
注意:
- 选主链时选择含碳官能团的最长碳链,并且从距离含碳官能团近的一端开始编号,其他规则和烷烃命名一致。这一点不光烯烃或炔烃使用,对于含有醛基羧基等的有机物同样使用。
- 当含碳官能团在
号位命名也可以省略其位置。
示例:
例如,下图中的烷烃,首先选用含有碳碳双键的最长碳链为主链,再从距离碳碳双键最近的一端对主链上的碳原子进行编号定位,命名为
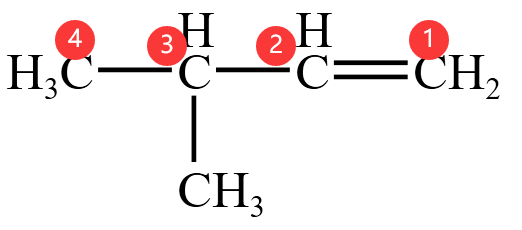
同理,下图中的炔烃,命名为
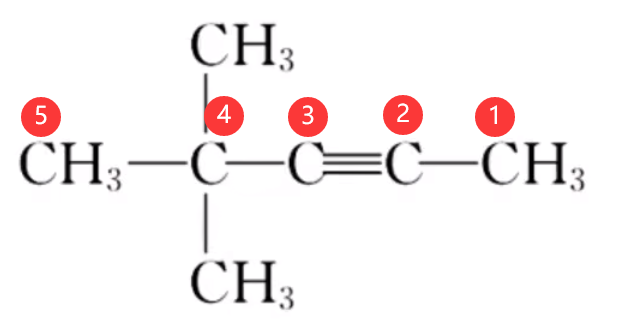
注意:
烯烃或炔烃需要用阿拉伯数字写出碳碳双键的位置。
选择主碳链时,一定要包含所有的双键,例如下图中的烯烃,只能选用编号链作为主链,同时考虑到要使得取代基乙基的编号较小,所以应该命名为
乙基 丁二烯。 所以有时候选用的并非原烯烃中最长的链。 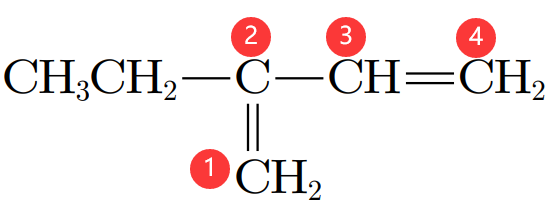
碳碳双键需要考虑顺反异构体。顺反异构,又名几何异构,属于立体异构中的一种。顺反异构是指化合物分子中由于具有自由旋转的限制因素,使各个基团在空间的排列方式不同而出现的非对映异构现象。如图所示,若
且 则存在顺反异构。若相同原子团在同一侧,则称为顺式;若在不同侧,则称为反式。 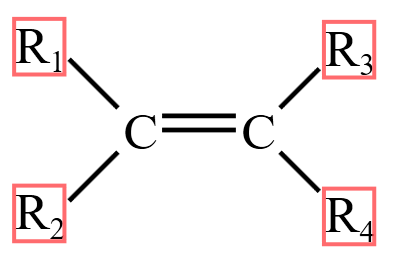
例如,下面左图中的烯烃由于上面的两个碳原子在同一侧,所以就是顺式,称为顺
丁烯;而右图中烯烃由于碳原子在不同侧,所以就是反式,称为反 丁烯。 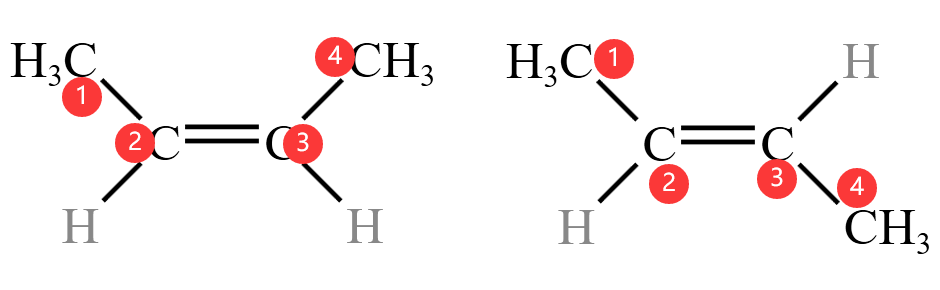
烃的衍生物命名规则
步骤
- 选母体:将含有官能团的最长碳链作为主链,称为「某烯」「某醇」「某醛」或「某酸」等。
- 编序号:从距离官能团最近的一端对主链碳原子进行编号。例如
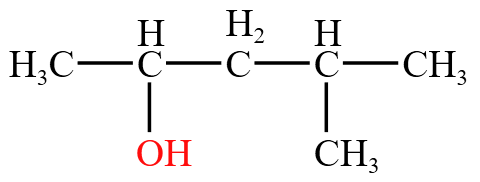 这个有机物中,羟基
这个有机物中,羟基 - 写名称:将支链作为取代基,写在「母体」名称的前面,并用阿拉伯数字标明支链和官能团的位置。
注意:
- 取代基要写在官能团前面。
- 若分子中同时含有双键(三键)和官能团,则选含有官能团和双键(三键)的最长碳链作为主链,根据主链上的碳原子数目称为「某烯(炔)醛」「某烯(炔)酸」。
- 若芳香环上连有取代基,则从官能团(羧基或醛基)所连的碳原子开始编号,使取代基的位次最小。
- 二元羧酸(或醛)命名时,选择含有两个羧基的最长碳链作为主链,然后根据主链碳原子的数目称为某二酸(醛)。
【总结】含官能团的有机物系统命名时,选主链、编号位要围绕官能团进行,且要注明官能团的位置及数目。
官能团的数目
含有两个或两个以上相同官能团的有机物命名要称之为「某二……」「某三……」,不能称之为「二某……」「三某」。如 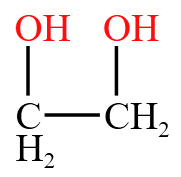 命名为「乙二醇」,而非「二乙醇」;
命名为「乙二醇」,而非「二乙醇」;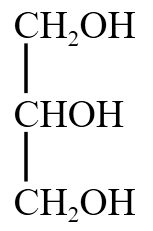 命名为「丙三醇」;再如
命名为「丙三醇」;再如 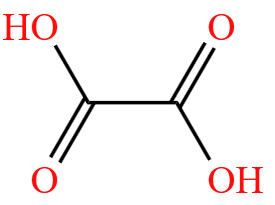 命名为乙二酸,也叫草酸;
命名为乙二酸,也叫草酸;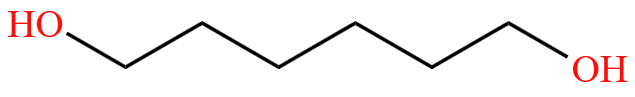 命名为
命名为
高中常见的官能团优先次序表
排在前面的是命名较优先的官能团。
简记:羧酯和酰胺,醛醇酚和胺,三双后有苯,烷基卤硝基。
除了硝基以外,含有
元素的官能团优先于含有 的官能团,含有 的官能团优先于没有 的官能团。含有两个 的羧基和酯基优先于含有一个 和一个 的酰胺,又优先于只有一个 的醛基、醇羟基、酚羟基,再优先于只有一个 的胺基。
在多官能团分子中,以顺序大为主官能团作为命名的母体类别,并以此确定起点位置,对碳链编号,顺序小的为次官能团,作为取代基进行命名,基本原则与烷烃类似。
例如,下图的有机物,将氨基作为取代基进行命名,称为
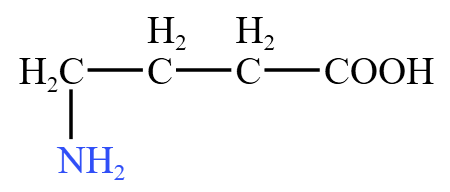
若是碳碳双键(或碳碳三键),组合羧基、醛基、羟基等,可以形成例如烯酸、稀醛、烯醇等,例如
酯类命名
根据
例如,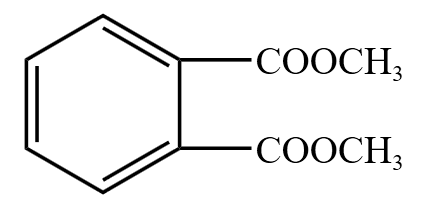 用习惯命名法命名为邻苯二甲酸二甲酯,即它是由邻苯二甲酸和二甲酯得到的。
用习惯命名法命名为邻苯二甲酸二甲酯,即它是由邻苯二甲酸和二甲酯得到的。
示例
例 1:下图中的有机物,应该按照编号作为主碳链,将甲基写在羟基前面,所以命名为
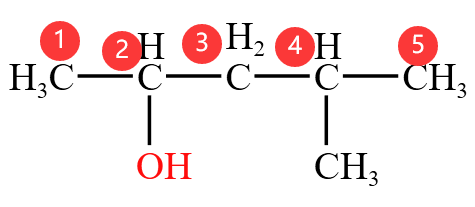
同理,下图中的有机物,应该命名为
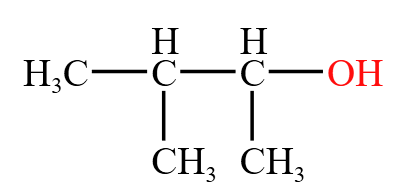
例 2:下图左边的有机物,对主碳链从左到右编号,羟基在第二个碳上,命名为
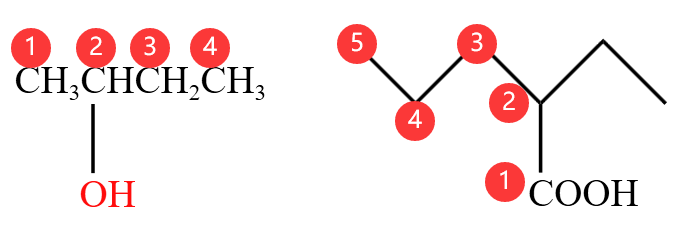
例 3:下图中的有机物,由六个碳构成了一个环,所以叫环己醇,那么考虑编号位顺序,从羟基所在的碳开始顺时针编号,则命名为
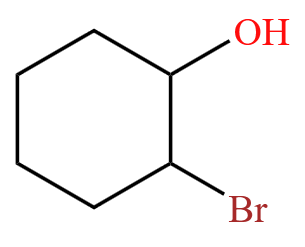
例 4:对于有机物
例 5(酯类命名):下图所示的有机物,由于含有酯基,根据 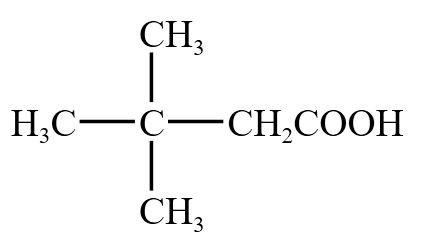 和甲醇
和甲醇
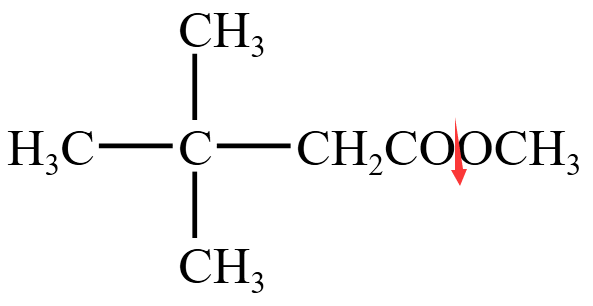
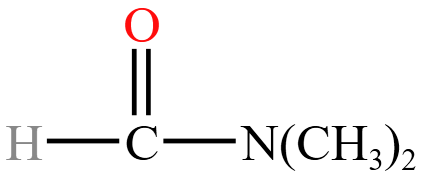
例 6:如图所示的有机物,相当于甲酰胺 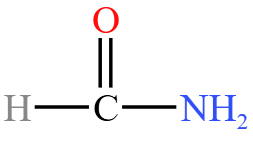 中两个氢原子被两个甲基取代,所以可命名为
中两个氢原子被两个甲基取代,所以可命名为
苯的同系物的命名
苯的同系物相关介绍
苯的同系物一般有两个条件:
- 结构中只有一个苯环。
- 侧链只有烷基。
习惯命名法
习惯命名法命名时,烷基的「基」可省略。
- 若为一元烷基取代(一元取代物),则可根据侧链取代基的名称,直接命名为「某苯」,例如甲苯、乙苯。
- 若苯环上仅有两个取代基(二元取代物)时,可分别用「邻」「间」和「对」来表示两取代基的相对位置,并用「相对位置 + 取代基名称 + 苯」命名。
系统命名法
-
若烷基相同,则以其中一个烷基所在的
-
若烷基不同,则以最简单的烷基所在的
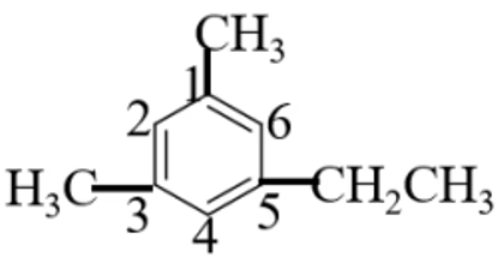
-
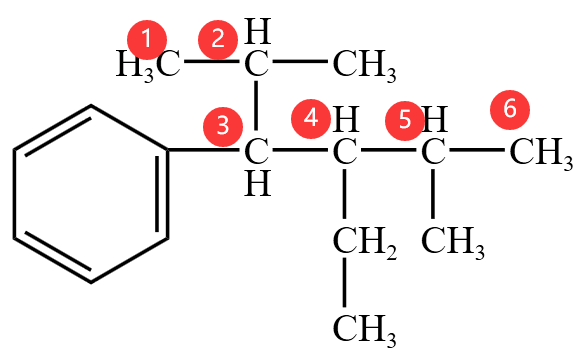
若苯环的侧链较复杂时,或苯环上含有不饱和烃基时,命名时一般把苯环作取代基,将较长的碳链作主链进行命名。此时选取主碳链的原则与之前烷烃、烯烃和炔烃相同。例如下图中的有机物,命名为
示例
| 结构简式 | 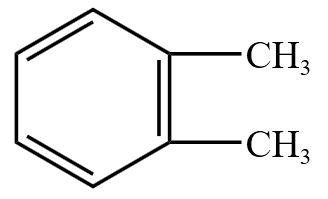 |
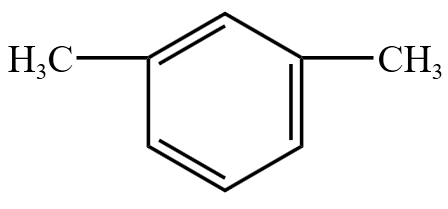 |
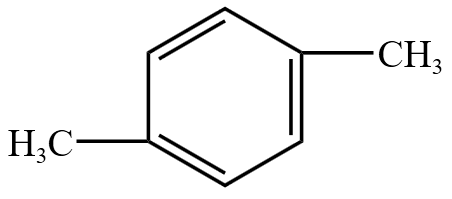 |
|---|---|---|---|
| 习惯名称 | 邻二甲苯 | 间二甲苯 | 对二甲苯 |
| 系统名称 |
注意:邻二甲苯也可以命名为邻二甲基苯,但习惯上省略「甲」。
含苯结构的有机物命名
根据上文取代基(官能团)的优先等级可知:
-
若苯的侧链为烷基、
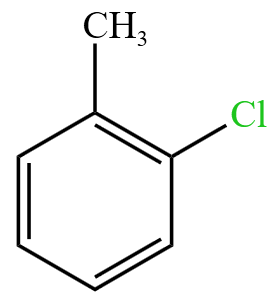
-
若苯的侧链为其它取代基/官能团,由于其它官能团优先级更高,所以其他官能团为母体,苯为取代基。下图是常见的苯为取代基的有机物。注意:羟基
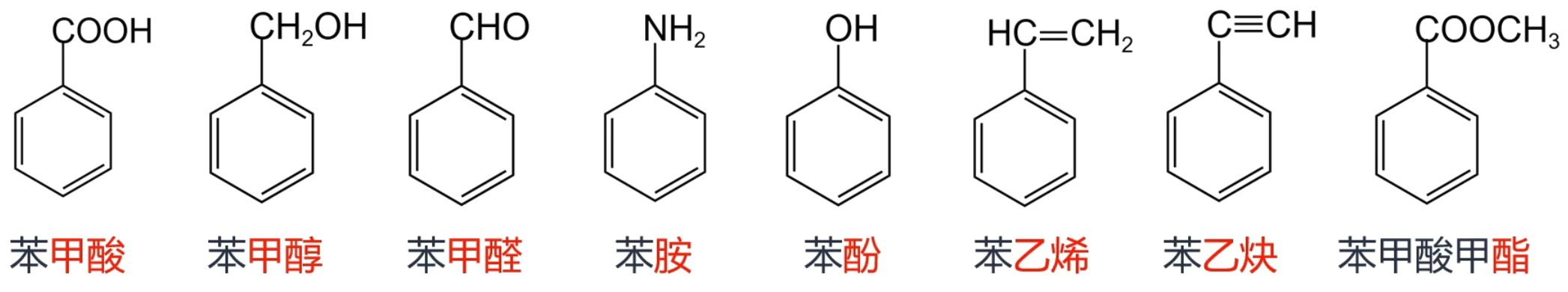
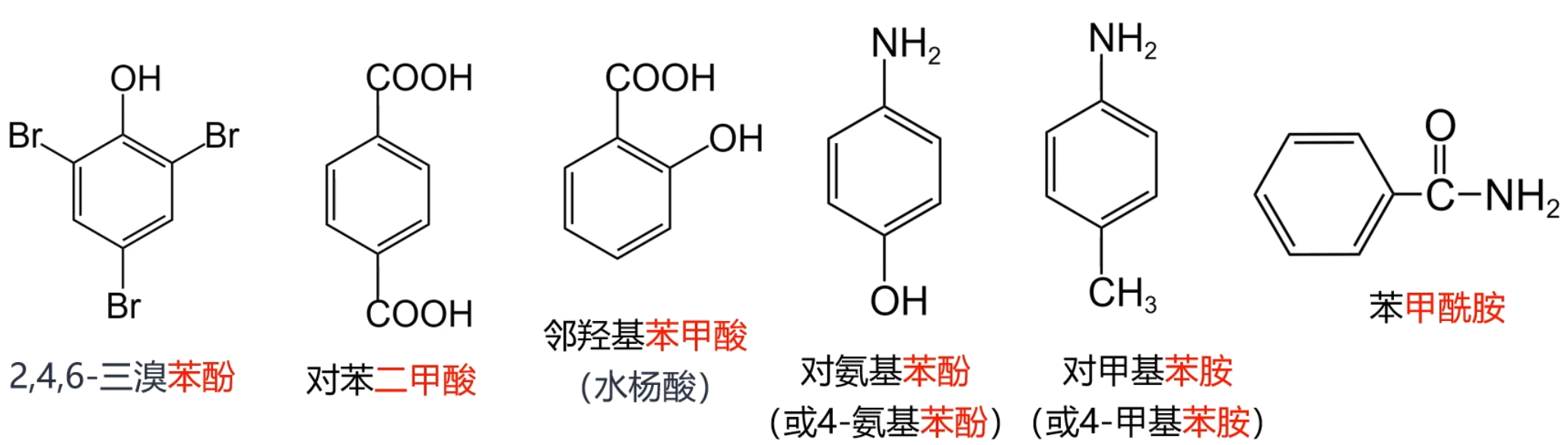
说明:
对于对苯二甲酸的命名:首先考虑主体是「甲酸」,由于羧基有两个,所以是「二甲酸」,再考虑到两个羧基在苯环上的位置是相对的,所以应该是「对苯二甲酸」。
如下图所示,该有机物含有酯基,是酯类,可以发现它是由对苯二甲酸
和甲醇
得到的,所以命名为对苯二甲酸甲酯。 邻羟基苯甲酸的知识:酰基
中若
为乙基,则是乙酰基 ,若邻羟基苯甲酸中
由乙酰基替换,则会得到乙酰水杨酸,如下图所示。乙酰水杨酸俗名是阿司匹林,所以阿司匹林显酸性。服用过多阿司匹林可能会对肠胃造成负担。 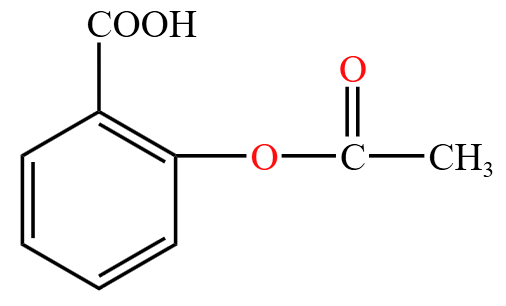
有机物命名新规则
根据中国化学会修订的《有机化合物命名规则 2017》,有机物中文名与其英文名大致保持一致。
情况一
不同方向最近支链位次相同时,按照英文字母首字母顺序确定优先级,例如
实例:下方有机物用旧命名规则命名为
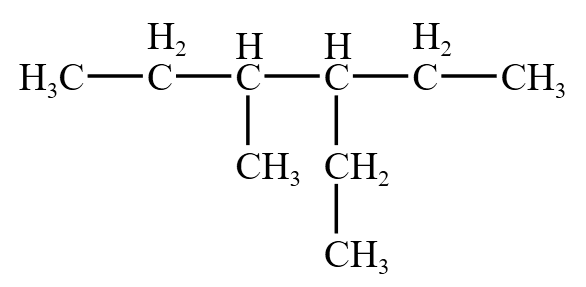
情况二
官能团位次紧挨官能团。例如: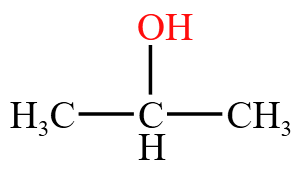 旧命名法为
旧命名法为
同分异构体
取代法求同分异构体
适用范围
适用于醇、醛、羧酸的同分异构体。
方法
将羟基、醛基、羧基直接看氯原子,直接找有机物的取代物种数几位同分异构体种数。
例如:链状有机物
第一步计算分子
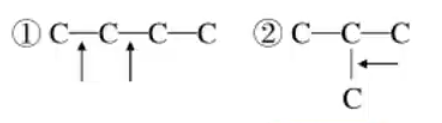
注意:这里第 ② 种结构无论碳碳双键在哪个键上都是等效的,因为旋转可重合。
接着对丁烯的结构进行一取代(将羟基作为一个整体取代原有机物上的氢),除去等效情况,即可得到
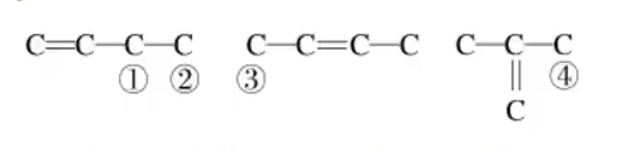
注意:碳碳双键不能和烃基直接相连,因为二者如果直接相连会相互作用生成醛基
,是不稳定的结构。
再如
研究有机化合物的一般方法
研究有机化合物的基本步骤
分离、提纯
有机化合物的分离、提纯
蒸馏
【原理】利用有机物与杂质的沸点差异,将有机化合物以蒸汽的形式蒸出,然后冷凝得到产品。
【适用对象】互相溶解、沸点不同的液态有机混合物。
【适用条件】
- 有机物的热稳定性较强。
- 有机物与杂质的沸点相差较大(一般约大于
【仪器(六件套)】蒸馏烧瓶/圆底烧瓶 + 三通管、酒精灯、温度计、直行冷凝管、尾接管(牛角管)、锥形瓶(接收器)。
【实验装置】
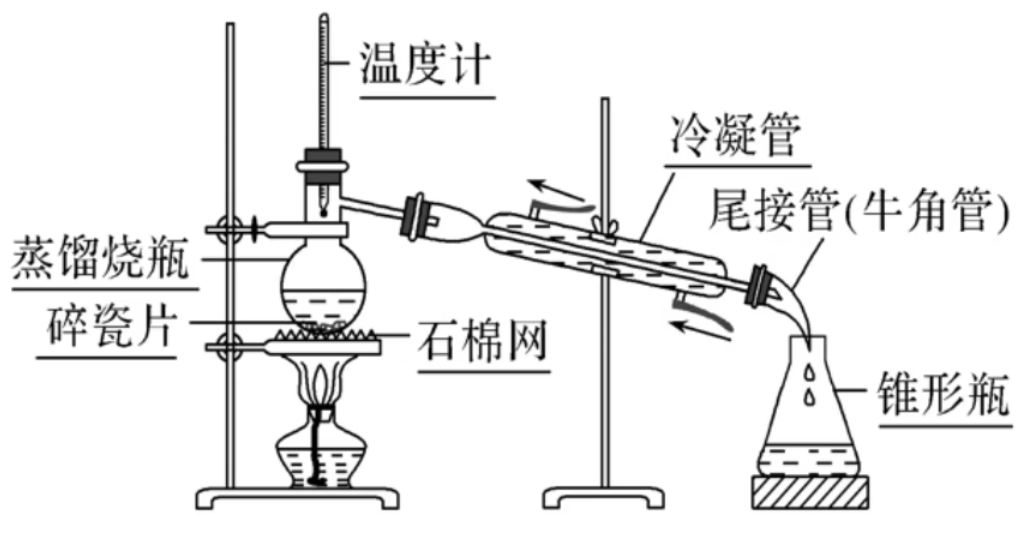
一般将两混合物
【相关考点&注意事项】
- 蒸馏烧瓶中盛液体的用量不超过
- 蒸馏烧瓶加热时需要石棉网。目的:均匀加热。
- 碎瓷片或沸石的作用:防止暴沸。
- 温度计下方小球的位置必须与蒸馏烧瓶支管口平齐,严格来说是球的上缘与支管口下缘相切。原因:测的是
- 冷凝管必须用直行冷凝管,不能用球形冷凝管。原因:球形冷凝管有很多凹槽,冷凝液体会停在凹槽中,无法收集到锥形瓶中。
- 冷水从下口进,上口出。原因:冷水流向与蒸汽流向相逆时,拥有最佳冷凝效果。
- 收集冷凝后的液体应该用锥形瓶,不能用烧杯。原因:烧杯口径过大,有可能会使得收集到的液体再次气化。
- 实验开始时,应该先通冷凝水,后加热;实验结束时,应该先停止加热,后停止通冷凝水。即冷凝水「先进后出」。
- 蒸馏虽然常用于分离、提纯液体有机物,但不一定都是液体和液体分离,还有可能是固体和液体分离,例如:无水乙醇的制备中,会有
萃取
【原理】
- 液 - 液萃取:利用待分离组分在两种不互溶的溶剂中溶解性不同,使待分离组分从溶解度小的溶剂中转移到溶解度较大的溶剂中。
- 固 - 液萃取:用溶剂从固体物质中溶解出待分离组分。
【萃取剂的选择原则】
- 与原溶剂互不相溶;
- 与溶质、原溶剂均不反应;
- 溶质在萃取剂中的溶解度远大于原溶剂;
- 萃取剂易于回收,一般沸点不高。
【常用萃取剂】乙醚
【流程】
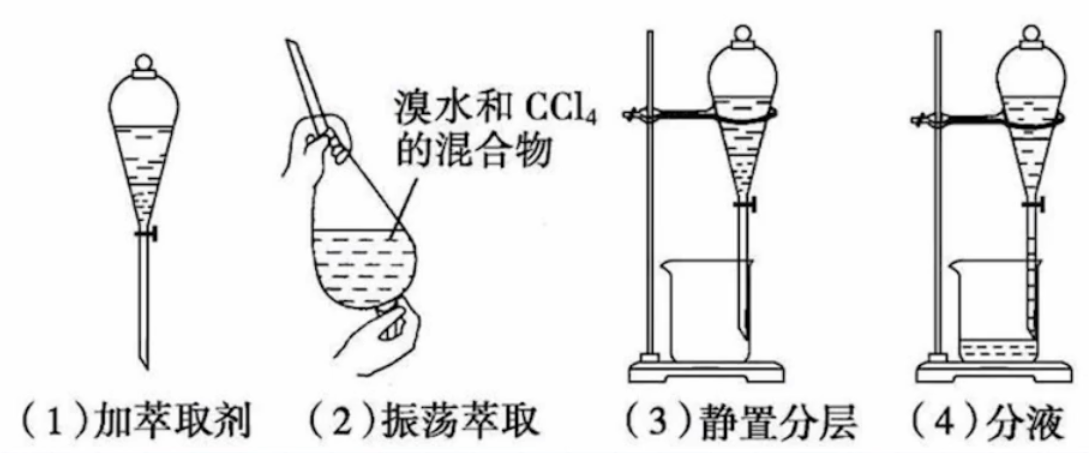
分液
【定义】将萃取后的两层液体(互不相溶、密度也不同的两种液体)分离开的操作方法。
【主要仪器】分液漏斗。
【实验装置】
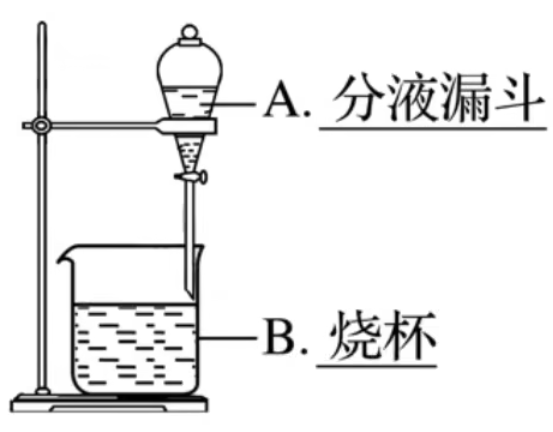
操作步骤:检漏
【相关考点&注意事项】
- 分液漏斗使用之前必须检漏。
- 使用时需将漏斗上口的玻璃塞打开,或使玻璃塞上的凹槽对准分液漏斗上的小孔。原因:为了保证漏斗内外压强相等,液体顺利流出。
- 漏斗下端管口紧靠烧杯内壁,分液时下层液体从下口流出,上层液体从上口倒出。
- 震荡时,分液漏斗倒置。
重结晶
【原理】利用被提纯物质与杂质在同一溶剂中的溶解度不同,而将杂质除去。(注意与萃取区分)
【适用对象】固体有机化合物。
【溶剂选择】
- 要求杂质在此溶剂中溶解度很小或溶解度很大,易于除去。
- 被提纯的有机化合物在此溶剂中的溶解度受温度的影响较大,能够进行冷却结晶。
注意:如果重结晶所得的晶体纯度不能达到要求,可以再次进行重结晶以提高产物的纯度。且纯度越高,产率越低。
【示例——重结晶法提纯苯甲酸】
-
实验目的:提纯含有少量氯化钠和泥沙杂质的苯甲酸。
-
资料:纯净的苯甲酸为无色结晶,其结构可表示为
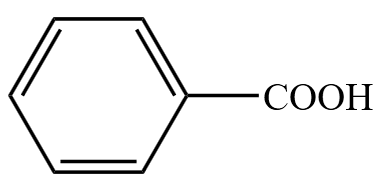 。熔点
。熔点 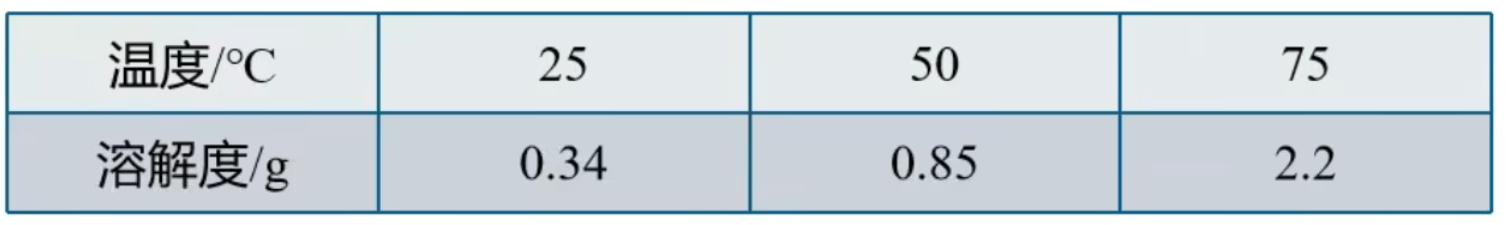
-
实验操作:粗苯甲酸
趁热过滤的原因:由于苯甲酸在水中的溶解度随着温度升高而升高,所以只有在温度较高时过滤,才能保证过滤出的杂质含有的苯甲酸较少,即避免苯甲酸因降温析出,影响产率。
注:由于氯化钠溶解度随温度变化很小,苯甲酸溶解度随温度变化很大,那么冷却结晶时,溶液中就会大量析出苯甲酸,一般很少析出氯化钠,从而达到提纯苯甲酸的目的。
色谱法
原理:利用吸附剂对不同物质的吸附作用不同,从而实现分离。
有机化合物的实验式确定
元素分析
定性分析:确定有机物的元素组成。
定量分析:确定有机物的实验式。
实验式
有机化合物分子内各元素原子的最简整数比,也称为最简式。
实验式与分子式的关系:分子式
鉴定有机物分子中的元素组成(定性分析)
将某有机物在
若将有机物完全燃烧,生成物只有
测定有机物中各元素的质量分数(定量分析)
实验式的测定步骤(李比希法):
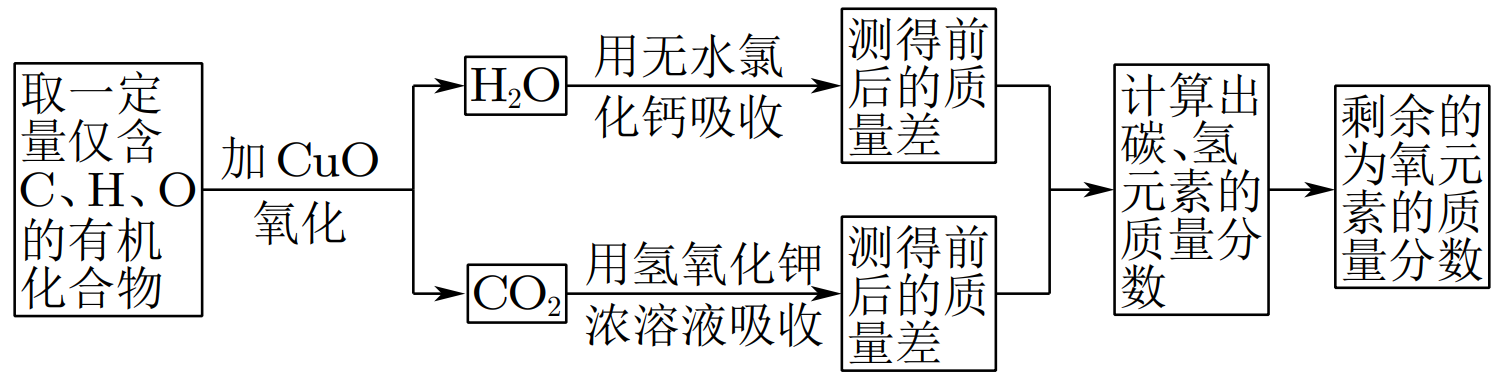
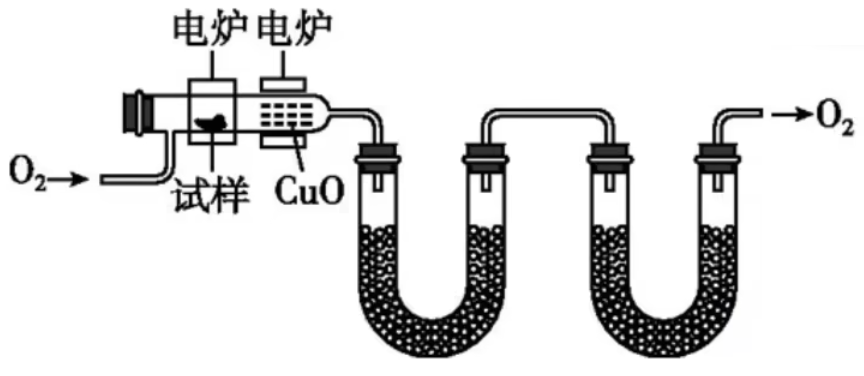
说明:二氧化碳除了用氢氧化钾浓溶液吸收外,还可以用碱石灰吸收,此时一定要先放入用于吸收水的
,再放入碱石灰,顺序不可颠倒。原因:如果碱石灰放在前面,则碱石灰会同时吸收掉二氧化碳和水蒸气,无法测出二氧化碳和水分别的增加量,从而无法测出碳氢元素的质量占比。
例 1:假设某种含
则氧的质量分数就是
小技巧:计算三者原子个数比时,可以用占比最小的去除以其它两个,比如上述例子中,用氧的含量表达式除以碳的含丽江表达式大约可以计算出碳是氧的两倍。
例 2:
分析:由题意可得
所以
所以有机物中
有机化合物的分子式确定
质谱法
元素定量分析
其中,求相对分子质量最精确、快捷的方法是「质谱法」。
质谱仪用高能电子流等轰击样品,使有机分子失去电子,形成带正电荷的分子离子和碎片离子等。这些离子因质量不同、电荷不同,在电场和磁场中的运动行为不同。计算机对其分析后,得到它们的相对质量与电荷数的比值,即质荷比。
质谱图:以质荷比为横坐标,以各类离子的相对丰度为纵坐标,根据记录结果所建立的坐标图。如下图为某有机物的质谱图:
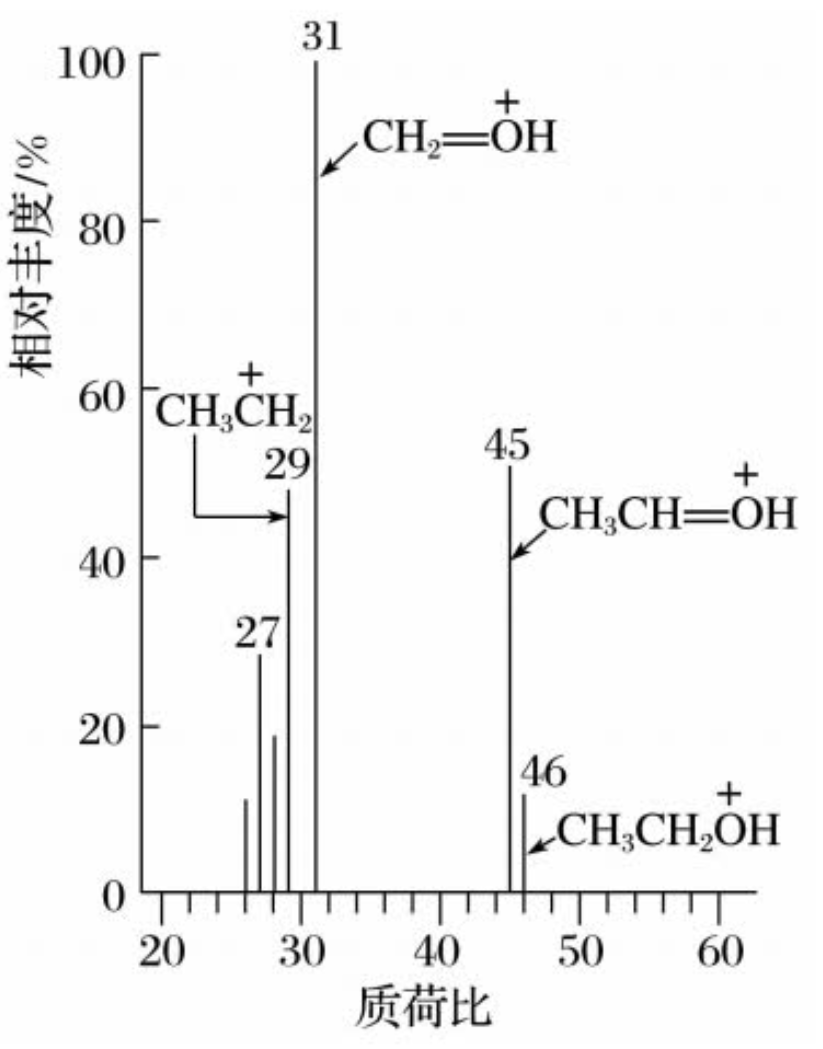
从图中可知,该未知物 A 的相对分子质量为
确定分子式:根据 分子式
相对密度法
做法:根据
例:某烃蒸气在相同条件下对氢气的相对密度为
分析:
已知
同时,根据
标况下密度法
做法:根据题目已知的标况下密度,以及标况下气体的摩尔质量为
例:某烃再标况下密度为
分析:
由题意可得
有机化合物的分子结构(结构式)确定
若确定某有机物分子式为
红外线光谱
作用:初步判断某有机物分子中所含有的化学键或官能团。
原理:不同的化学键或官能团的吸收频率不同,在红外光谱图上将处于不同的位置。
例如:分子式为
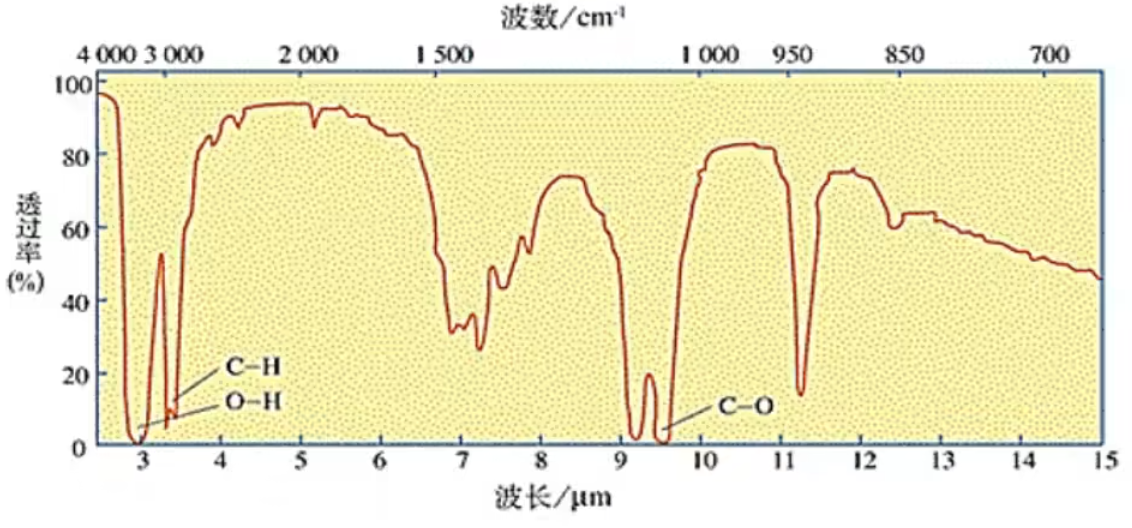
应用:可获得分子中所含有的化学键或官能团的信息,从而明确有机化合物中的分子结构。
核磁共振氢谱
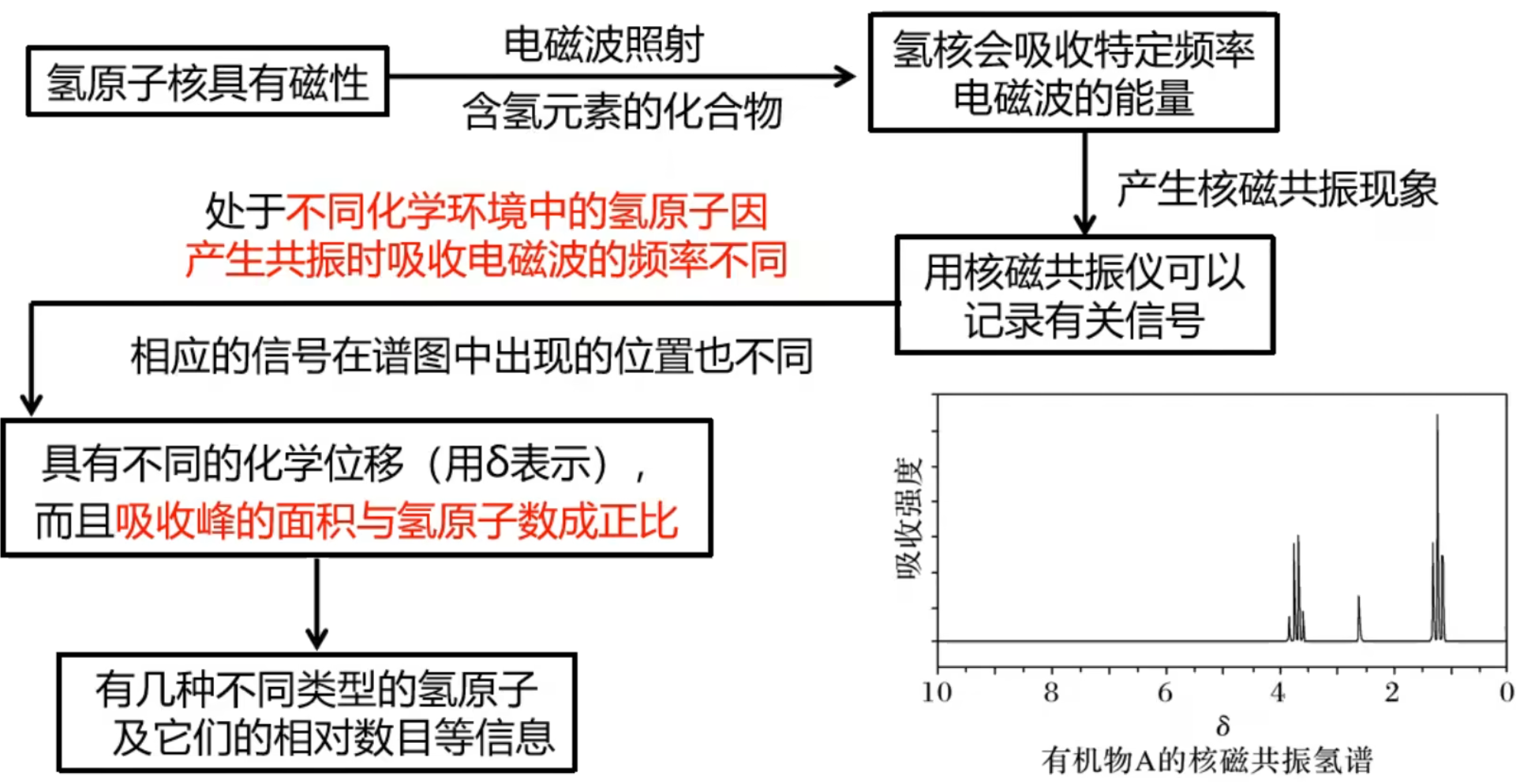
核磁共振氢谱中,峰的组数代表等效氢的种类数,而峰面积比代表具体个数比。
举例——分子式为
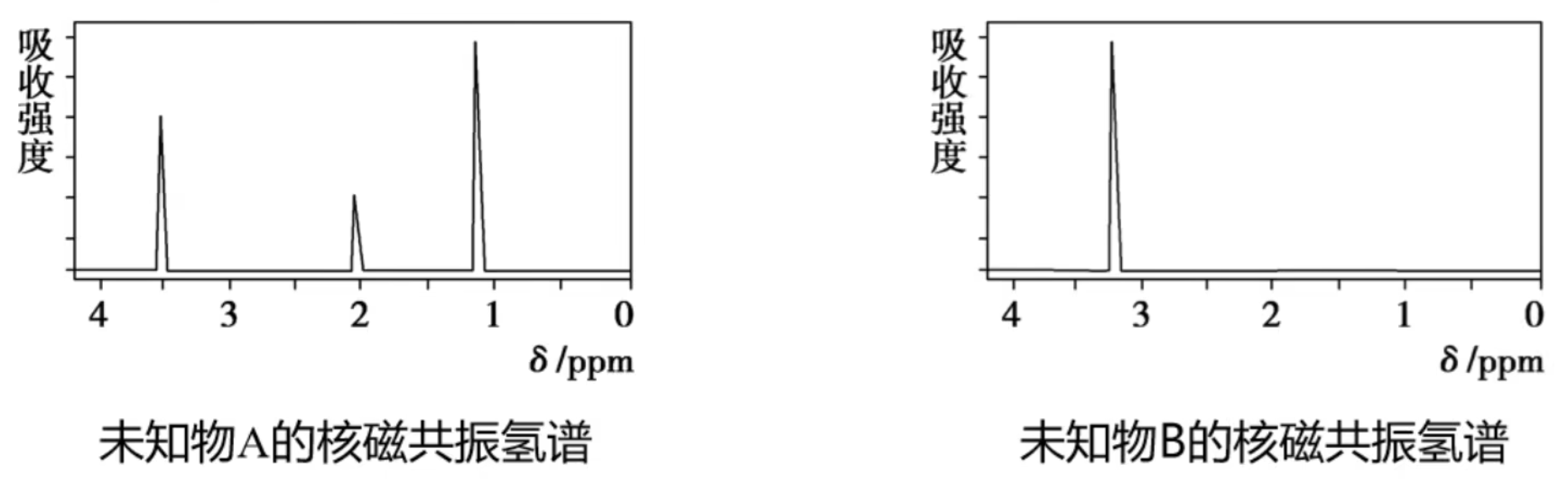
上图中未知物 A 和 B 的分子式都是
观察图可发现,未知物 A 分子中有 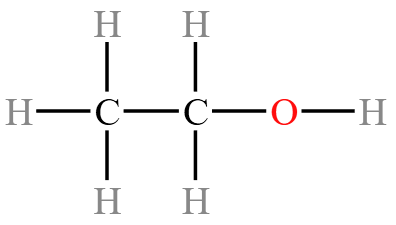 ,其中
,其中
同理,未知物 B 分子中的 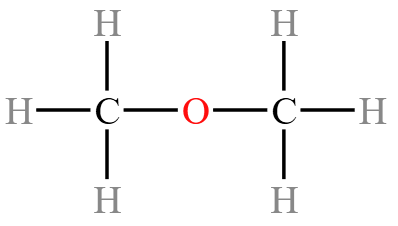 ,即六个
,即六个
其它示例:
对二甲基苯的结构式为
,其结构上下左右均对称,有两种不同化学环境下的氢原子,其中六个氢原子接在侧链对称的碳上,这是第一种化学环境,这六个氢原子等价;除此之外,苯环上还接了
个 ,这四个氢原子等价,属于第二种化学环境。
X 射线衍射(XRD)
【原理】X 射线是一种波长很短(约
【适用范围】只适用于晶体。
【应用】将 X 射线衍射技术用于有机化合物(特别是复杂的生物大分子)晶体结构的测定,可以获得更为直接而详尽的结构信息。
其它方法
【化学方法】
一般根据有机物的化学性质推出。
例:若烃 A 分子式为
【有机物的结构特点】
可根据有机物的结构特点判断。
例:已知烃 B 的分子式为 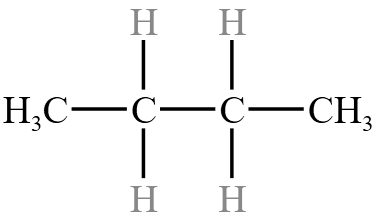 ;实验式分别为
;实验式分别为
【常见官能团特征反应】
| 官能团种类 | 试剂 | 判断依据 |
|---|---|---|
| 碳碳双键/三键 | 溴的 |
橙红色褪去 |
| 碳碳双键/三键 | 酸性 |
紫色褪去 |
| 卤素原子 | 有沉淀产生 | |
| 醇羟基 | 钠 | 有氢气放出 |
| 酚羟基 | 显紫色 | |
| 酚羟基 | 浓溴水 | 有白色沉淀产生 |
| 醛基 | 银氨溶液 | 有银镜产生 |
| 醛基 | 新制 |
有红色沉淀产生 |
| 羧基 | 有 |
注意:醇不和碳酸氢钠反应,只能与钠反应;羧酸酸性大于碳酸,所以羧基可以与碳酸氢钠反应生成
。高中阶段能与碳酸氢钠反应生成气体的只有羧基。
总结
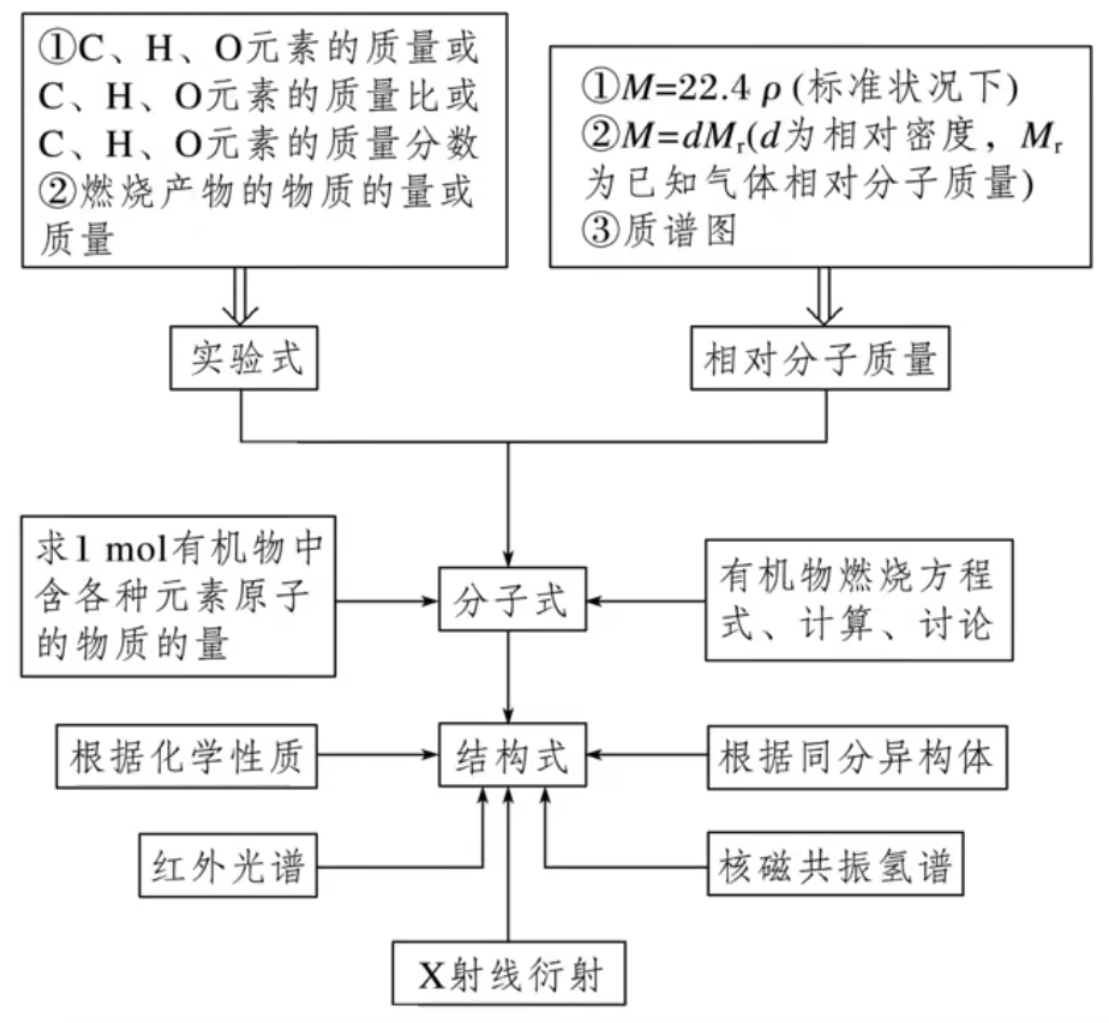
谱图法在确定有机物分子结构中的应用:
- 核磁共振氢谱图:峰的个数即氢原子的种类数,而峰面积之比为各类氢原子个数之比。
- 红外光谱图:推知有机物分子中含有哪些化学键、官能团,从而确定有机物的结构。
- X 射线衍射技术:用于有机化合物(特别是复杂的生物大分子)晶体结构的测定。



【推荐】国内首个AI IDE,深度理解中文开发场景,立即下载体验Trae
【推荐】编程新体验,更懂你的AI,立即体验豆包MarsCode编程助手
【推荐】抖音旗下AI助手豆包,你的智能百科全书,全免费不限次数
【推荐】轻量又高性能的 SSH 工具 IShell:AI 加持,快人一步
· 分享4款.NET开源、免费、实用的商城系统
· 全程不用写代码,我用AI程序员写了一个飞机大战
· MongoDB 8.0这个新功能碉堡了,比商业数据库还牛
· 白话解读 Dapr 1.15:你的「微服务管家」又秀新绝活了
· 记一次.NET内存居高不下排查解决与启示
2022-07-01 【题解】P5322 [BJOI2019] 排兵布阵(DP,背包)