Cancer Cell | 肿瘤微环境渐进式调控AML治疗抵抗的分子机制
急性髓系白血病 ( acute myeloid leukemia, AML ) 是成年人常见的血液系统恶性肿瘤之一,主要表现为髓系原始细胞克隆性恶性增殖及正常造血细胞功能抑制。在AML基因突变图谱中,fms样酪氨酸激酶3 ( fms-like receptor tyrosine kinase 3, FLT3 ) 基因突变最为常见,存在于约1/3初诊AML患者。FLT3突变形式主要包括跨膜区内部的串联重复突变 ( ITD ) 和累及活化环中的点突变( TKD ) 两种形式。虽然这些突变影响细胞功能的分子机制尚不清楚,但大量临床研究已表明,携带FLT3突变的AML患者预后不良,这也催生了一系列FLT3抑制剂 (FLT3i) 的研发及临床运用。
FLT3i尽管可以有效地清除外周循环血中的白血病细胞,但部分AML细胞仍可存在于骨髓微环境中,这种现象被称为早期抵抗 (early resistance),这些残存的细胞在受到分子刺激后还会引起AML持续发展。遗憾的是,出现早期抵抗的细胞数量极少,只有当这些细胞不断增殖导致肿瘤复发,也被称为晚期抵抗 (late resistance) 时,才能着手加以研究,很大程度上限制了对于AML细胞整个治疗抵抗发展过程及相关分子特征的认识。
Gilteritinib是一种强效FLT3i,FDA批准其用于治疗患有复发或难治性AML成人患者。近日,来自俄勒冈健康与科学大学的Elie Traer教授团队,利用蛋白基因组学 (proteogenomics) 研究策略系统分析了gilteritinib治疗引起的AML治疗抵抗全过程中细胞基因组、蛋白质组、磷酸化修饰组等方面分子功能的变化。相关结果以“The AML microenvironment catalyzes a stepwise evolution to gilteritinib resistance" 为题 [1] ,发表于Cancer Cell。

01肿瘤微环境引起的AML细胞治疗抵抗
研究人员利用纤维母细胞生长因子FGF2或FLT3配体FL分别与gilteritinib共同刺激MOLM14细胞 (人AML FLT3-ITD+细胞系) 约4个月的时间 ,以模拟AML患者接受gilteritinib治疗时,骨髓微环境对AML细胞的保护作用。FGF2和FL分别通过激活MAPK/PI3K/AKT信号、恢复FLT3活性,有效地启动AML细胞早期治疗抵抗效应,逆转glitertinib对细胞的杀伤作用。4个月后去除FGF2和FL,gilteritinib仍可短暂抑制AML细胞生长,但随后,细胞MAPK/PI3K/AKT信号再次激活导致晚期治疗抵抗现象,这一现象由于不再依赖任何FGF2或FL,因此也被称作配体非依赖的晚期治疗抵抗 (ligand-independent late resistant)。
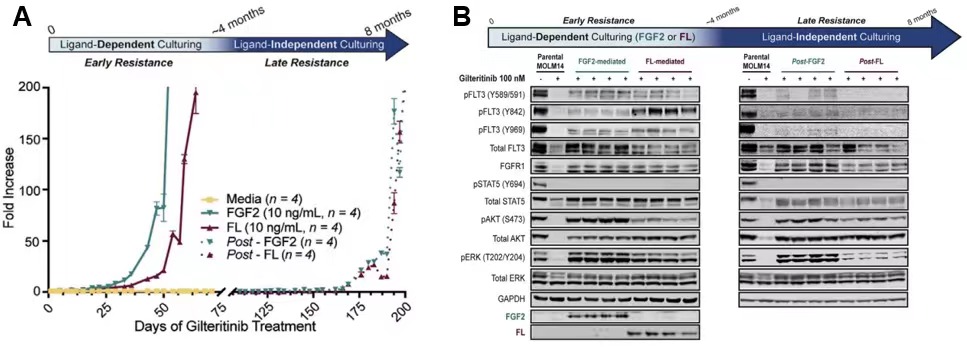
图1 FGF2和FL对AML细胞gilteritinib治疗敏感性的影响
02NRAS突变与AML细胞晚期抵抗相关性
全外显子测序 (WES) 结果显示,晚期治疗抵抗MOLM14细胞以及基因编辑产生的gilteritinib耐药细胞系MV4;11都出现了多种NRAS点突变。构建的MOLM14NRASG12S/D突变细胞则在初期对gilteritinib治疗十分敏感,提示NARS突变不足以立即引起细胞耐药,但却可以引起配体非依赖的晚期治疗抵抗;另一方面,FGF2或FL也能提前治疗抵抗发生时间,强调了肿瘤微环境对细胞治疗效果影响的重要性。
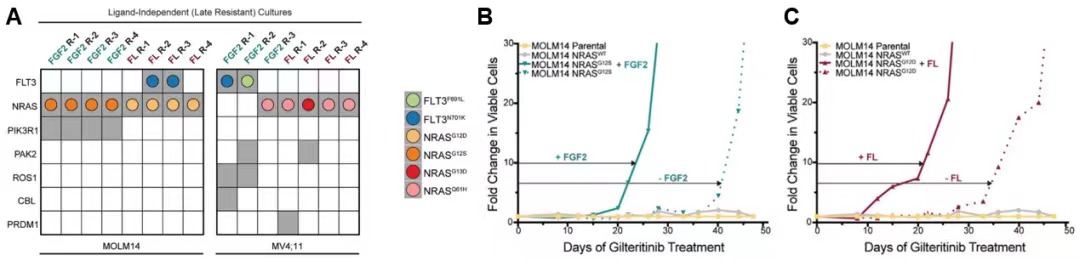
图2 NARS突变对AML细胞glitertinib治疗敏感性的影响
03AML细胞治疗抵抗过程中蛋白质功能改变
随后,结合蛋白质组学、磷酸化修饰组学技术,研究人员在MOLM14亲代细胞和早期、晚期gilteritinib治疗抵抗细胞中一共鉴定到了7694个蛋白质和36004个磷酸化肽段。主成分分析 (PCA) 显示,不同类型细胞的 (磷酸化) 蛋白质特征明显彼此区分;激酶-底物富集分析 (KSEA) 表明,在AML细胞出现早期治疗抵抗时,与细胞周期发展相关的激酶 (CDK1, 2, 4, 5, 6, 7, 9) 活性明显降低,而细胞周期检查点 (PRKCA, CSNK2A1)、DNA损伤反应调控相关激酶活性则升高;上述现象在晚期治疗抵抗中明显反转,表现为CDK家族激酶活性升高。从CausalPath信号通路分析也可以看出,早期抵抗时AML细胞周期信号通路活性明显降低,而在后期,CDKs和MAPK相关信号通路活性则显著增强。
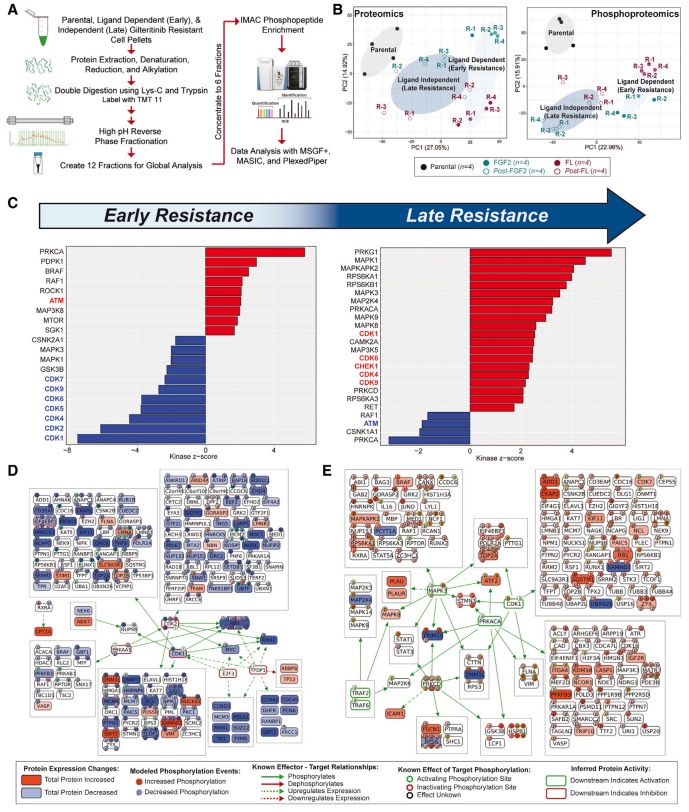
图3 AML细胞早期/晚期治疗抵抗过程中蛋白质及磷酸化修饰水平的改变
04细胞周期调控AML早期治疗抵抗
FGF2和FL刺激导致早期耐药的MOLM14细胞与亲代细胞相比,进入S期的细胞数量明显减少,而G2/M期细胞数量却未发生明显改变,提示细胞周期停滞;晚期出现治疗抵抗的细胞周期状态则与未处理的亲代MOLM14细胞类似。细胞周期激酶Aurora 参与细胞有丝分裂过程中染色体的调节、胞质分裂和动粒-微管连接等。研究人员发现Aurora激酶B (AURKB) 抑制剂 (AZD2811) 以及CRISPR/Cas9敲除AURKB都增强了AML细胞早期对gilteritinb的敏感性,证明了AURKB调控AML早期细胞耐药。
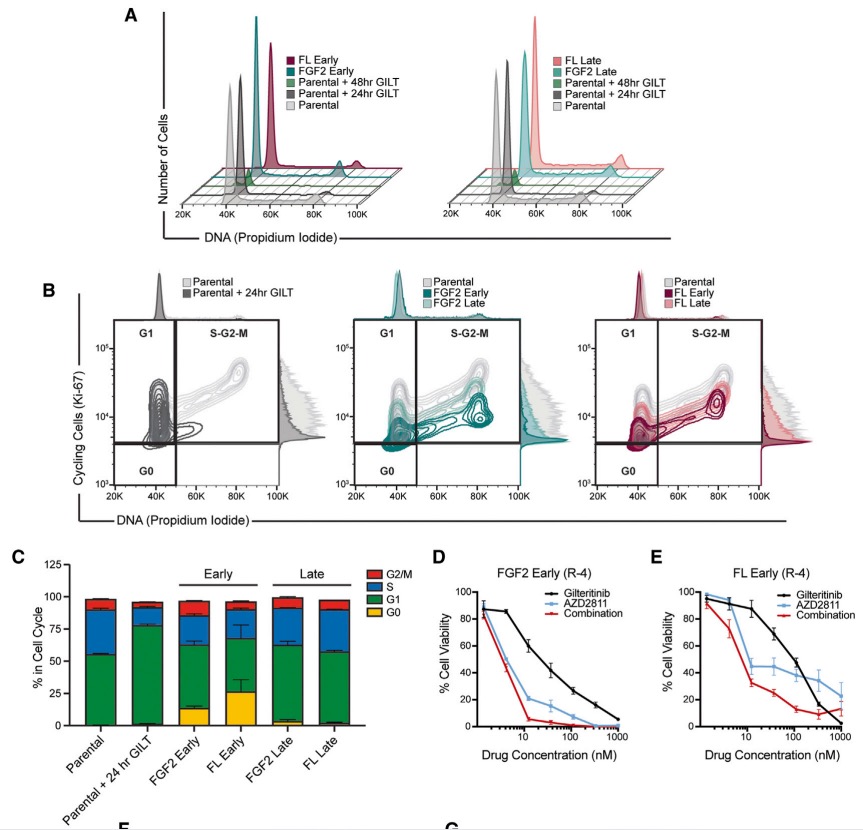
图4 细胞周期对AML治疗抵抗的影响
05AML细胞治疗抵抗过程中蛋白质功能改变
最后,研究人员利用靶向蛋白质组学技术分析了11例临床AML患者,在经gilteritinib治疗前后,白血病细胞 (CD33+ CD34+) 中123个蛋白质含量变化的情况。其中,52个蛋白质含量在gilteritinib治疗后出现了明显改变,这些蛋白质主要为:(1)调控细胞周期进程的蛋白质含量明显减少,包括CDK1/2/4/9;(2)MAPK信号通路和脂肪酸代谢通路蛋白质增加。考虑到此前研究结果已证明AURKB在AML细胞系早期治疗抵抗中的重要作用,研究人员也进一步研究了AURKB抑制剂AZD2811对AML患者白血病细胞的影响,结果显示,AZD2811对治疗前的AML细胞gilteritinib敏感性影响不大,但是明显地提高了gilteritinib杀伤早期抵抗细胞的效果。更为重要的是,通过调研BeatAML数据库397例AML患者治疗数据,研究人员也发现FIT3-ITD突变AML患者对AZD2811治疗更敏感,但进展到晚期出现NARS突变的患者则对AZD2811不敏感,侧面反映了抑制细胞周期调控激酶AURKB活性对扼制AML早期抗药性的重要性。
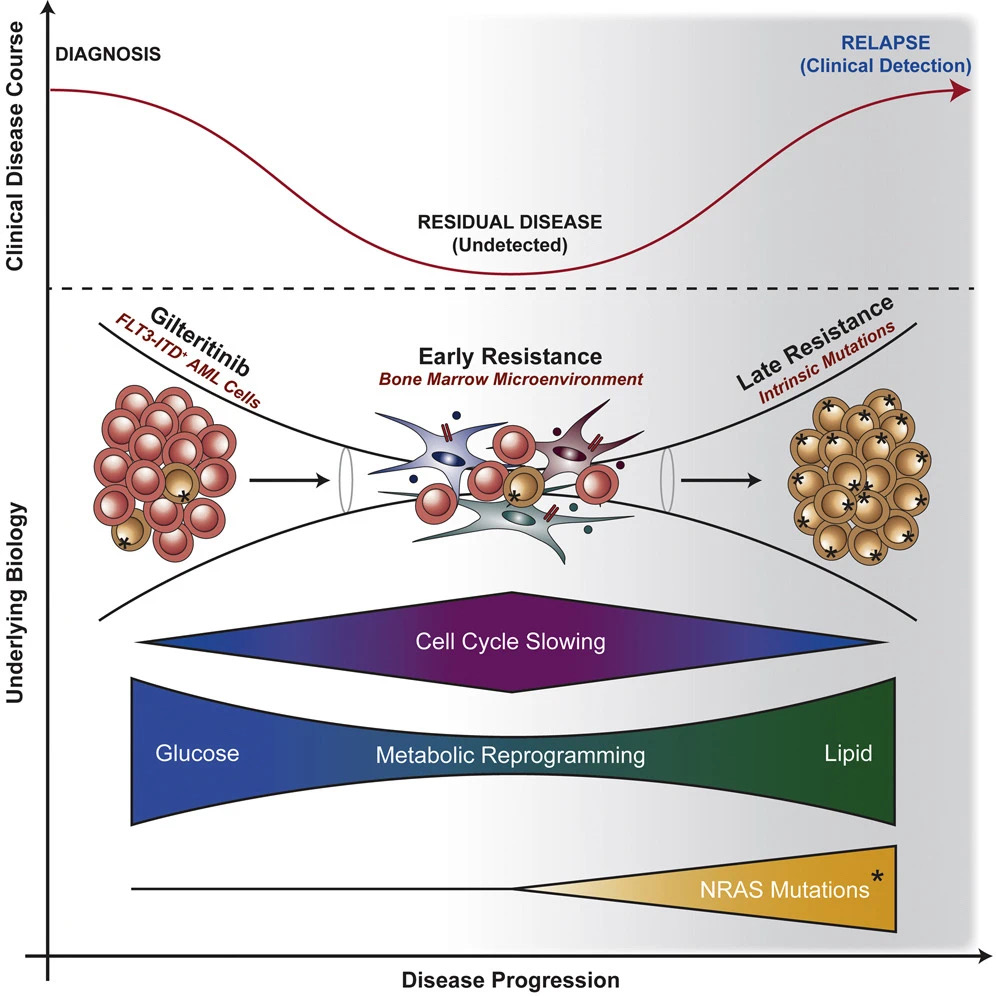
总的来说,此项研究证实了AML细胞在经gilteritinib治疗后出现早/晚不同阶段治疗抵抗,在此基础上,利用基因组、蛋白质组、磷酸化修饰组学等技术详细研究了两个阶段细胞的分子特征,发现晚期NRAS突变,早期细胞周期相关激酶抑制等标志性事件,并结合AML患者细胞实验及大规模临床数据揭示了AURKB调控AML早期治疗抵抗的关键作用。这些结果也为实现AML的彻底根除奠定了重要基础。
参考文献:
Sunil K. Joshi, et al. 2021. The AML microenvironment catalyzes a stepwise evolution to gilteritinib resistance. Cancer Cell.



 浙公网安备 33010602011771号
浙公网安备 33010602011771号