乙烯和苯:知识预习
CH4含C量:75%。
C2H4含C量:85.7%。
C6H6含C量:92.3%。
========================================================================================================================
一、乙烯
分子式:C2H4。
电子式: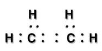 。
。
结构式:![]() 。
。
结构简式:H2C=CH2。
最简式:CH2。
空间结构示意图:暂无图片。
球棍模型: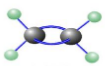 。
。
比例模型: 。
。
空间结构:平面形(键角:120°)。
性质:
物理性质:
无色稍有气味气体,密度略小于空气(ρC₂H₄ = 1.25g/mL),难溶于水(排水法)。
化学性质:活泼。
①氧化反应:
燃烧反应:
C2H4 + 2O2 -点燃-> 2CO2 + 2H2O。
现象:火焰明亮,伴有黑烟。
与酸性KMnO4aq反应:
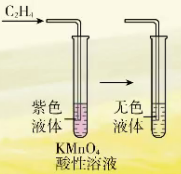
现象:酸性KMnO4aq褪色。
②加成反应:
定义:有机物中的双键或三键两端的C直接与其他原子或原子团结合生成新的化合物的反应。
与Cl2(氯气/液氯/氯水/氯气的四氯化碳溶液/氯气的苯溶液)反应:
CH2=CH2 + Cl2 -> CH2Cl-CH2Cl(1,2-二氯乙烷)。
现象:氯水褪色。
与Br2(溴蒸气/液溴/溴水/溴的四氯化碳溶液/溴的苯溶液)反应:
CH2=CH2 + Br2 -> CH2Br-CH2Br(1,2-二溴乙烷)。
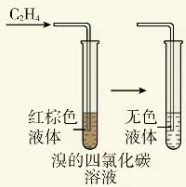
现象:溴水褪色。
与H2:
CH2=CH2 + H2 -催化剂(Ni或Pt或Pd)-△-> CH3-CH3(乙烷)。
与HCl:
CH2=CH2 + HCl -催化剂-△-> CH3-CH2Cl(氯乙烷)(工业制氯乙烷)。
与HBr:
CH2=CH2 + HBr -> CH3-CH2Br(溴乙烷)。
与H2O:
CH2=CH2 + H2O -催化剂-高温高压-> CH2-CH3-OH(乙醇)(工业制乙醇)。
注:
①加成1mol双键消耗1molCl2/Br2/H2/HCl/HBr/H2O。
②1molC2H4与足量Cl2/Br2/H2/HCl/HBr/H2O反应,最多消耗1molCl2/Br2/H2/HCl/HBr/H2O。
③聚合反应
别称:加成聚合反应、加聚反应。
nCH2=CH2(单体) -一定条件(引发剂、催化剂)-> -[-CH2-CH2-]-n(聚合度)。
口诀:平面无色难溶水,一燃两褪得记对,酷爱加成四物质,唯有卤素无条件。
鉴别CH4、C2H4:①酸性KMnO4aq,②溴水。
CH4(C2H4):足量溴水。
应用:催熟剂。
=========================================================================================
二、苯
分子式:C6H6。
电子式:不作要求。
结构式: 。
。
注:C6H6中不含单键、双键,含大π键。
结构简式: (凯库勒式)、
(凯库勒式)、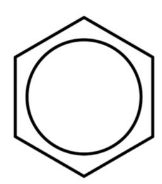 。
。
最简式:CH。
空间结构示意图:暂无图片。
球棍模型: 。
。
比例模型: 。
。
空间结构:平面正六边形(键角:120°)。
性质:
物理性质:
无色具有特殊气味有毒液体,密度小于水,不溶于水,易挥发,沸点低(沸点:80.1℃)。
化学性质:易取代,能加成,难氧化。
①氧化反应:
燃烧反应:
2C6H6 + 15O2 --点燃> 12CO2 + 6H2O。
现象:火焰更明亮,浓烈黑烟。
②取代反应:
溴(溴蒸气/液溴)代反应:
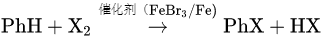 。
。
溴苯(无色油状液体,密度大于水,溶解Br2呈棕红色)。
硝化反应:
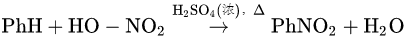 。
。
硝基苯(无色苦杏仁味油状剧毒液体,密度大于水)。
③加成反应:
与H2反应:
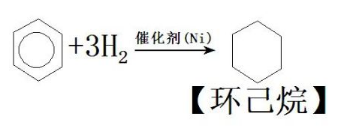 (六氢化苯)
(六氢化苯)
C6H5Br(Br2):足量NaOHaq。
Br2 + 2NaOH = NaBr + NaBrO + H2O。
本文来自博客园,作者:临化银,转载请注明原文链接:https://www.cnblogs.com/luotei/p/14346589.html
——蘸以清墨,书我弦歌。

 浙公网安备 33010602011771号
浙公网安备 33010602011771号