Metabolic Signatures of Cystic Fibrosis Identified in Dried Blood Spots For Newborn Screening Without Carrier Identification (文献分享一组-孔楠楠)
题目:Metabolic Signatures of Cystic Fibrosis Identified in Dried Blood Spots For Newborn Screening Without Carrier Identification(新生儿筛查(不含携带者鉴定)中使用干血片鉴定囊性纤维化的代谢特征)
期刊:Journal of Proteome Research
发表时间:December 3, 2018
DOI:10.1021/acs.jproteome.8b00351
分享人:孔楠楠
技术:非靶向代谢组学
概述:
本研究通过使用有质量控制的多段注射-毛细管电泳-质谱(MS)高通量平台对有体积限制/生物标记的囊性纤维化(CF)样品进行非靶向代谢物分析,首次报道了从单个3.2 mm直径的干血片(DBS)中鉴定到的一组CF特异代谢物。这项工作为生命早期的CF代谢表型提供了新的视角,对于更好地理解未知临床表现的编码囊性纤维化跨膜传导调节因子(CFTR)突变以及开发更准确且低成本的CF筛选策略是必需的。
背景:
囊性纤维化(CF)是一种复杂的多器官疾病,是由编码囊性纤维化跨膜传导调节因子(CFTR)的基因突变而引起的,是早期治疗干预中最常见的致命常染色体隐性遗传疾病之一。近几年来,可在第一次衰弱症状发作之前进行CF的治疗干预已被纳入新生儿筛查(NBS)计划之中。目前用于CF发病前检测的新生儿筛查(NBS)依赖于两阶段免疫反应性胰蛋白酶原(IRT)和囊性纤维化跨膜传导调节因子(CFTR)突变组算法,即对2日龄新生儿干血片(DBS)中升高的免疫胰蛋白酶原(IRT)和DNA突变组进行检测,然后对所有推定的SP病例进行验证性汗液检测。但是,由于IRT阈值和CFTR突变总数的显着差异,该算法虽然敏感但筛查阳性不确定诊断(CF-SPID)病例的频率仍高于诊断预期。即使使用浮动临界值进行IRT的校正和使用最佳IRT / DNA算法进行CF筛查,CF整体阳性的预测值(PPV≈4.5%)仍低于通过串联质谱(MS / MS)对其他遗传疾病进行的新生儿筛查,例如苯丙酮尿症。因此,是否可以开发一种高成本效益、高准确的方法进行CF的筛选,以更好地为临床决策提供信息?
由于代谢物是基因表达和环境暴露的“真实世界”终产物,代谢组学为精确医学需要在生物标志物鉴定上的突破提供了一种有效的方法。代谢组学不仅用于鉴定潜伏的早期阶段临床相关的疾病生物标志物,也可以提供疾病病理生理机制的新见解,并揭示“沉默”基因突变的表型。因此,人们越来越关注应用代谢组学来表征CF的代谢表型。例如,使用液相色谱-质谱(LC-MS)和气相色谱-质谱(GC-MS)的血清代谢组学研究显示CF患儿的能量代谢改变反映了异常的中枢能量代谢,氧化应激和肠道微生物群活动。类似地,对CF和非CF患者培养的人气道上皮细胞的代谢组学分析证实了已知的氧化和渗透压力的改变。
因此,在这项工作中,使用高通量平台——多段注射-毛细管电泳-质谱(MSI-CE-MS),首次从无胎儿肠梗阻、无症状的新生儿DBS提取物中鉴定到一组CF特异性代谢物,将有利于更准确地筛查人群中受影响的CF新生儿。
实验设计:


结果:
本研究对三组新生儿的DBS提取物进行了代谢组学研究,即确认的CF病例,SN(筛选阴性)/健康和SP(筛选阳性,如携带者和高胰蛋白酶原者)/非CF对照,未包括早产儿/重症患儿,所有新生儿均为正常胎龄(38-42周)和出生体重(> 2500 g)。总体而言,在MSI-CE-MS中,可以在大多数DBS样本(> 75%)中可靠地检测到70种阳离子代谢物。所有已知的代谢物都是通过掺入真实标准品鉴定的,而未知代谢物的结构解析则是通过高分辨率MS和MS / MS进行的。
这项回顾性病例对照研究通过与胎龄/性别匹配的筛选阴性对照SN /健康新生儿对照(n = 44)相比,校正了错误发现率(q <0.05)之后,在没有胎粪性肠梗阻的正常出生体重CF新生儿中(n = 36)鉴定到了32种差异表达的代谢物,包括一系列N-糖氨基酸,氧化型谷胱甘肽二硫化物和烟酰胺。此外,在有CFTR突变和短暂高胰蛋白酶原反应的筛选阳性新生儿携带者(n = 72)中,来自DBS提取物的16种代谢物可以区分真正的CF病例。重要的是,从三个独立批次的DBS标本鉴定出的6个符合Bonferroni校正(p <7.25×10-5)的候选CF特异性生物标志物,包括几个在循环中耗尽的氨基酸(Tyr,Ser,Thr,Pro,Gly),可能反映了蛋白质消化不良/吸收不良的现象。此外,由于外分泌腺/上皮组织的谷胱甘肽外流受损和与IRT直接相关的未知三价肽升高(ρ= 0.332,p = 4.55×10-4),CF新生儿中低含量的眼晶体酸含量可以作为表明氧化应激的指标。未知代谢物的结构解析通过高分辨率MS / MS完成,而生物标志物验证是通过利用在官方认可的NBS设施中进行直接进样的MS / MS分析来比较新生儿DBS样本的一系列代谢物实现。
本研究的第一阶段旨在通过收集出生后~2天的DBS样本的特征代谢表型,来鉴定出能够区分无症状CF新生儿和健康新生儿的生物标志物。然后,鉴定到区分CF新生儿与SP /非CF新生儿的差异代谢物。
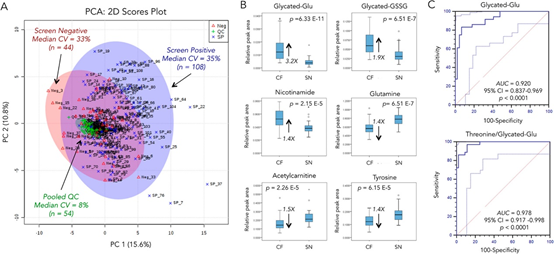
图A中主成分分析PCA的二维 2D评分图展现了新生儿代谢表型的概述。,通过SN /健康新生儿组内部紧密的QC样品簇(绿色,中值CV为8%)可以反映出优异的技术精度。正如预期的一样,来自一组SP /假定CF病例(n = 108,CV=35%)和SN /健康新生儿对照(n = 44,CV=33%)的DBS提取物之间具有更大的生物学差异。
图B描绘了与健康/筛选阴性对照(n = 44)相比,在高汗液氯化物(n = 36)的CF婴儿中鉴定到的差异代谢物的盒须图,其包括升高的N-糖基化谷氨酸(Glc-Glu)、糖化氧化型谷胱甘肽(Glc-GSSG)和烟酰胺,以及降低的谷氨酰胺(Gln)、乙酰肉碱和酪氨酸(Tyr)。
图C描绘了代谢物Glc-Glu和Thr/Glc-Glu比例的ROC曲线,表明可显著区分开CF新生儿与阴性对照(p <0.0001),曲线下面积(AUC)> 0.920。
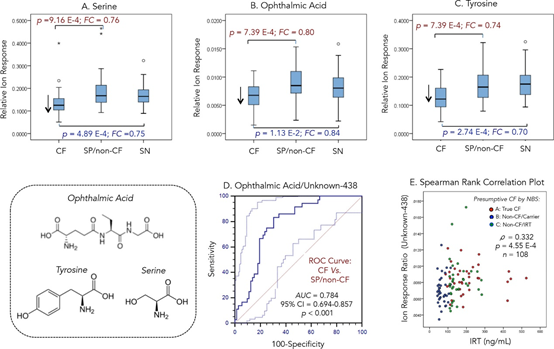
图A-C描绘了三种重要代谢物眼酸(ophthalmic acid,OPA),Tyr和丝氨酸(Ser)在三组新生儿中的盒须图。
图D显示OPA在CF新生儿与未受影响的SP /非CF病例的良好分化。有趣的是,未知肽的测量比率提供了良好的预测准确性(AUC = 0.784,p <0.001),以区分无症状CF新生儿与未受影响的携带者。
图E为斯皮尔曼等级相关分析,表明未知肽与IRT浓度正相关(ρ= 0.332,p = 4.55×10-4),提示它可能代表胰蛋白酶原激活的副产物。
总结:
这项工作提出了第一个非靶向代谢组学研究,用于回顾新生儿DBS标本的CF症状发生前检测。采用完全验证的代谢组学工作流程,采用严格的质量控制措施,可以以极高的技术精度对数据进行有效的批次校正。初步数据表明CF新生儿患有由外分泌胰腺功能不全引起的蛋白质消化不良/吸收不良,这反映在较低浓度的几种循环氨基酸(特别是Tyr,Ser和Thr),而OPA水平的降低表明CFTR功能障碍引起的谷胱甘肽外排受损。
目前仍需要前瞻性研究来验证CF特异性生物标志物对NBS的临床效用,可以使用现有的DI-MS / MS基础设施进行测量,作为提高NBS对CF的阳性预测值的一种方法。预计新生儿的代谢表型有助于解决CF中的其他诊断困境,包括未通过IRT筛查检测到的假阴性,具有未知或可变后果的CFTR突变的筛查阳性,以及诊断不确定且缺乏了解的推定CF病例预后。


 浙公网安备 33010602011771号
浙公网安备 33010602011771号