寒假笔记本4:锌
锌\(\rm Zn\),元素周期表30号,四周期IIB族。

\(\rm Part\ I.\ 锌的存在\)
单一的锌矿比较少,主要资源如下:
- 闪锌矿\(\rm ZnS\)
- 菱锌矿\(\rm ZnCO_3\)
- 红锌矿\(\rm ZnO\)
- 硅锌矿\(\rm Zn_2SiO_4\)
- 锰硅锌矿\(\rm (ZnMn)_2SiO_4\)
- 异极矿\(\rm Zn_4Si_2O_7(OH)_2·H2O\)(一水合碱式焦硅酸锌),非常好看的一种矿石

- 铅锌矿和铜锌矿(我国主要是这种)。
人们很早就知道锌的存在。作为人类最早知道的化合物——甚至用来治病——锌的单质却很晚才被提炼出来。最早提出的锌单质的提炼方法是在《天工开物》里提到。
有趣的是,1750~1850人们已经开始用氧化锌\(\rm ZnO\)和硫化锌\(\rm ZnS_2\)来治病。确实,锌也是“壮阳神器”。

\(\rm Part\ II.\ 理化性质\)
\(\rm \large I.\ 物理性质\)
锌是一种银白色略带淡蓝色金属,密度为\(\rm 7.14g/cm^3\),熔点为\(\rm 419.5℃\)
\(\large \rm II. \text{化学性质}\)
锌的化学性质和铝类似,主要氧化态+2,也有+1。在空气密度小于70%的时候,形成致密氧化膜\(\rm 2Zn+3H_2O(g)+CO_2\xlongequal{\ \ \ \ }Zn_2(OH)_2CO_3+2H_2\)
- 锌和氧族元素(O/S...)的反应
\(\rm Zn+O/S/...\xlongequal{加热}ZnO/ZnS/...\)
当然,直接反应除了氧气速率都很慢。硫化锌的制取方法一般是:
\(\rm ZnCl_2(aq)+H_2S(aq)\xlongequal{\ \ \ \ \ }ZnS+2HCl(aq)\) - 由于表面的氧化膜,锌和卤素(F/Cl/...)的反应会稍微慢一些
\(\rm Zn+Cl_2/I_2\xlongequal{高温}ZnCl_2/I_2\)
\(\rm ZnO + 2HBr(aq)\xlongequal{\ \ \ \ \ \ }ZnBr_2(aq)+H_2O(l)\) - 锌可以和酸(浓硫酸等除外)反应
\(\rm Zn+H-酸根\xlongequal{\ \ \ \ }Zn-酸根+H_2\uparrow\) - 锌可以和氢氧化钠溶液反应
\(\rm 2Zn_4NaOH(aq) \xlongequal{\ \ \ \ \ }2Na_2ZnO_2(aq)+H_2\uparrow\) - 锌的氢氧化物有两性,既可以和酸反应,也可以和碱反应
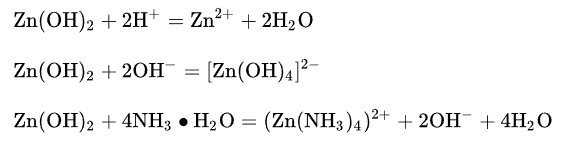
\(\rm Part\ III.用途\)
锌主要用于钢铁、冶金、机械、电气、化工、轻工、军事和医药等领域。
在现代工业中,锌是电池制造上有不可替代的,为一相当重要的金属。此外,锌也是人体必需的微量元素之一,起着极其重要的作用(男性可以多吃,有好处!)。


 浙公网安备 33010602011771号
浙公网安备 33010602011771号