Chem is why-[补档 3]
胶体
分散系
把一种(或多种)物质以粒子形式(这个比较重要,要不然什么东西不能说是分散系对吧) 分散到另一种(或多种)物质中的得到的体系,叫做 分散系。
前者是被称作 分散质,后者被称为 分散剂。显然,跟 溶质与溶剂 有那么一丝丝相像(看定义,溶液本来就是一种分散系)
一些例子:
- 溶液
- 有色玻璃(比如啤酒瓶的分散剂是玻璃,分散质可能是氧化亚铁)
- 粉钻(据杜岳说,其分散质是三氧化二钴)
- 牛奶
- 云、雾、烟
分散系分类
当分散剂为液体时,我们按照分散质粒子的 直径,对其进行分类。
| 分散质粒子直径 | 称呼 | 举例 |
|---|---|---|
| 溶液 | 溶液 | |
| 胶体 | 豆浆,蛋白质溶液,淀粉溶液(这两个有欺诈性的名称!蛋白质和淀粉都是有机物,属于高分子那一类,什么意思呢,高分子就是分子很巨大的意思,分子一大,就到了胶体的级别) | |
| 浊液 | 泥土水 |
为什么要这样分层呢?一定是由于胶体有一些不同于溶液和浊液的性质。
比方说呢,溶液比较稳定,而胶体处于一个 介稳 的状态,浊液则分层不稳定。
又比如说,下面要介绍的丁达尔效应!
丁达尔效应 Tyndall Effect
可见光通过胶体,从侧面可以看到光亮的通路。
这就是 丁达尔效应。
为什么呢?
我们知道,光是有 波粒二象性 的(不知道也没关系,听过就知道了),就是说他又是波,又是粒子。
下面是大画家 why 画的一些比较优美的图片:
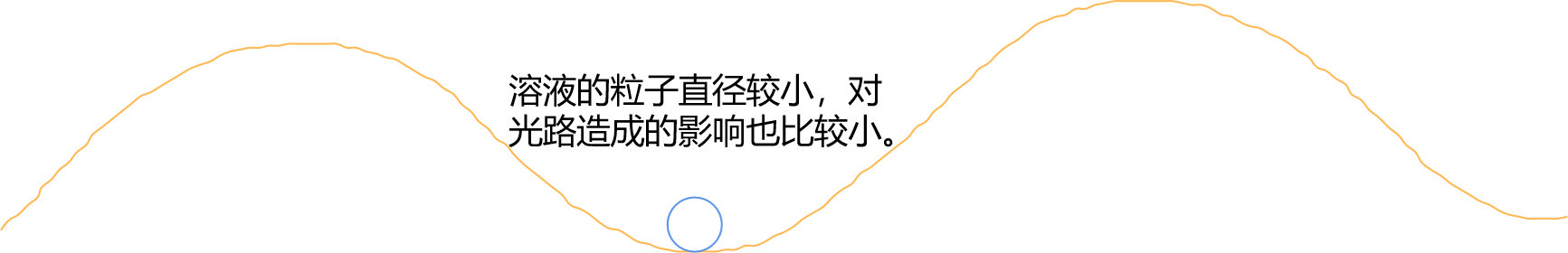
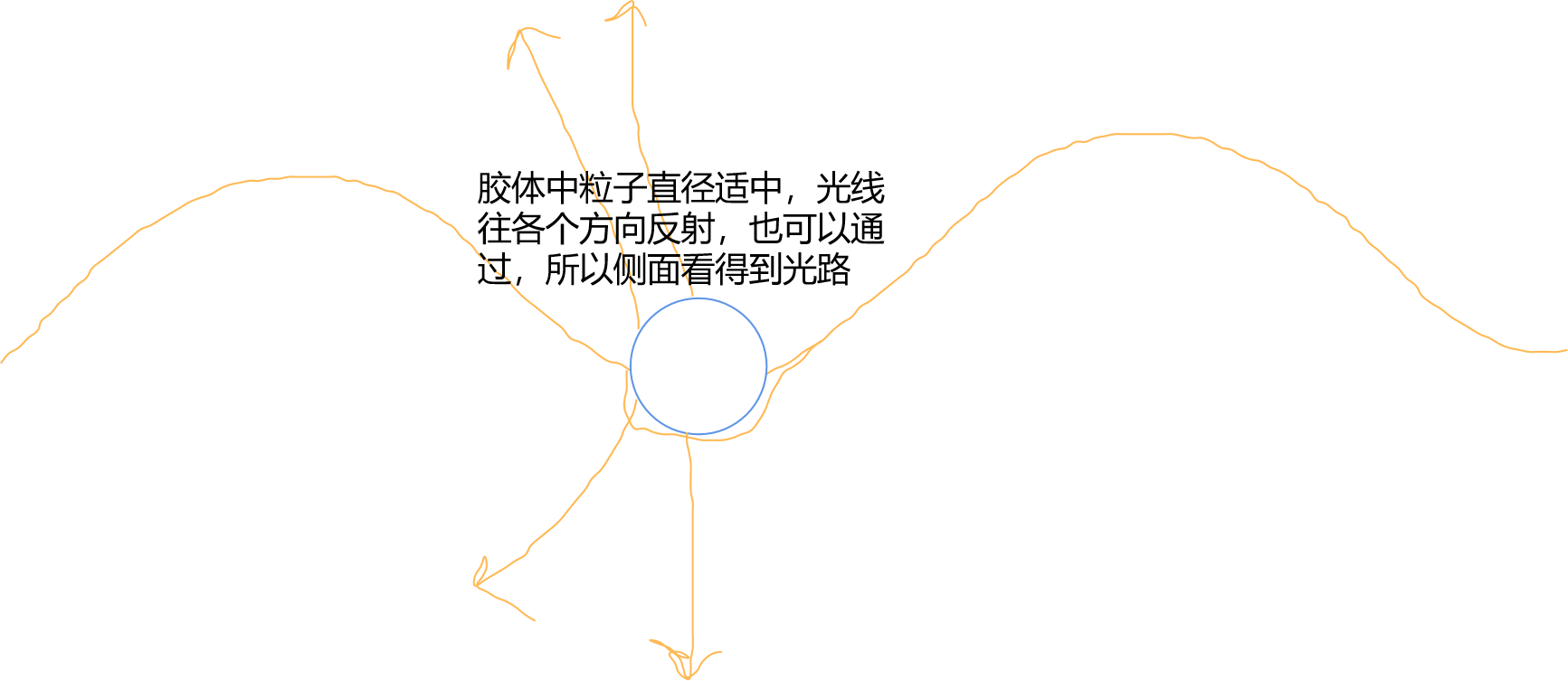

思考:丁达尔效应能不能用来判断一个分散系是不是胶体?
答案:不能! 因为胶体和溶液浊液的精细的区别是人为划定的。比方说分散质粒子直径 的分散系也许也会有比较弱的丁达尔效应,但是它就不是胶体。
制备 胶体
- 沸水中加入 滴 饱和溶液。
- 煮沸至红褐色。
发生的反应
你可能会好奇,这个反应怎么能发生啊!我们只学过逆向的那个反应啊。
没关系,因为我也一直很好奇。
这个东西叫做 盐类的水解。
(下面是我口胡的,绝对不保证正确性!!/youl)
就是说我这个 ,在水里之后会电离成 ,因为水会微弱电离出 ,而 和 各自独自美好,但是 和 却会结合生成 ,然后加热,一方面加快这个反应,另一方面,让易挥发的 挥发出来。想起来,国庆作业里有饱和 溶液通电制 。感觉有点相似性,但又不太相干。那个方程式是
聚沉现象
胶粒带着相同的电性,所以相互排斥,不会聚集吸引形成更大颗粒从而聚沉。
一般来说,氢氧化物胶粒带是正电,而黄河泥沙则是带负电。
那么怎么样会聚沉呢?
- 加入强电解质。增加水中的电荷,从而让胶粒更容易吸引。
- 加热/搅拌。增大胶粒撞在一起的可能。
- 加带相反电荷的胶体。
生活应用与现象解释:
- 胶体净水。金属胶体带正电,泥沙则带负电,从而吸引聚沉。常用的是明矾 。
- 卤水点豆腐。豆浆是胶体, 等强电解质加进去聚沉成为豆腐。
- 三角洲。可以理解为 海水点沙!河流裹挟着的泥沙就像豆浆是胶体,而海水中 等较多,所以泥沙就聚沉了!
实验室里的一个现象: 胶体逐滴滴加稀硫酸。现象是:先有红褐色沉淀,然后沉淀逐渐溶解。
电泳现象
在外加电场的作用下,带电胶粒定向移动。
B 站上截来的图片。
本文作者:LJC001151
本文链接:https://www.cnblogs.com/LJC001151/p/16753752.html
版权声明:本作品采用知识共享署名-非商业性使用-禁止演绎 2.5 中国大陆许可协议进行许可。








【推荐】国内首个AI IDE,深度理解中文开发场景,立即下载体验Trae
【推荐】编程新体验,更懂你的AI,立即体验豆包MarsCode编程助手
【推荐】抖音旗下AI助手豆包,你的智能百科全书,全免费不限次数
【推荐】轻量又高性能的 SSH 工具 IShell:AI 加持,快人一步